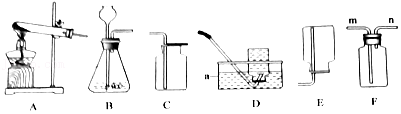
16.兴趣小组同学在做镁与盐反应的实验时,不小心将镁条加到饱和的碳酸氢钠溶液中,意外发现溶液中有白色不溶物生成。同学们对白色不溶物的成分产生了浓厚兴趣,于是在老师的帮助下进行了如下的探究。
【提出问题】白色不溶物是什么物质?
【猜想与假设】
猜想①是Mg(OH)
2猜想②是MgCO
3猜想③是Mg(OH)
2和MgCO
3的混合物
【查阅资料】
1、MgCO
3、Mg(OH)
2加热易分解,分别生成两种氧化物。
2、白色无水硫酸铜遇水变蓝。
3、碱石灰是固体氢氧化钠和氧化钙的混合物。
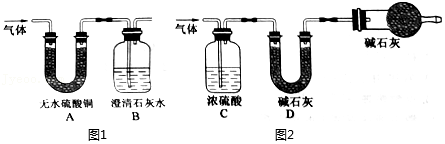
【实验验证】取适量干燥的白色不溶物,充分加热,并使分解产生的气体依次通过如图1所示装置。
(1)【实验现象】装置A中
,装置B中
。
(2)【实验结论】猜想③正确。请写出Mg(OH)
2受热分解的化学方程式
。
(3)【拓展探究】直接向白色不溶物中滴加足量
,也能检验MgCO
3的存在。
同学们为了进一步测定白色不溶物中各组分的质量关系,继续进行了下列探究。
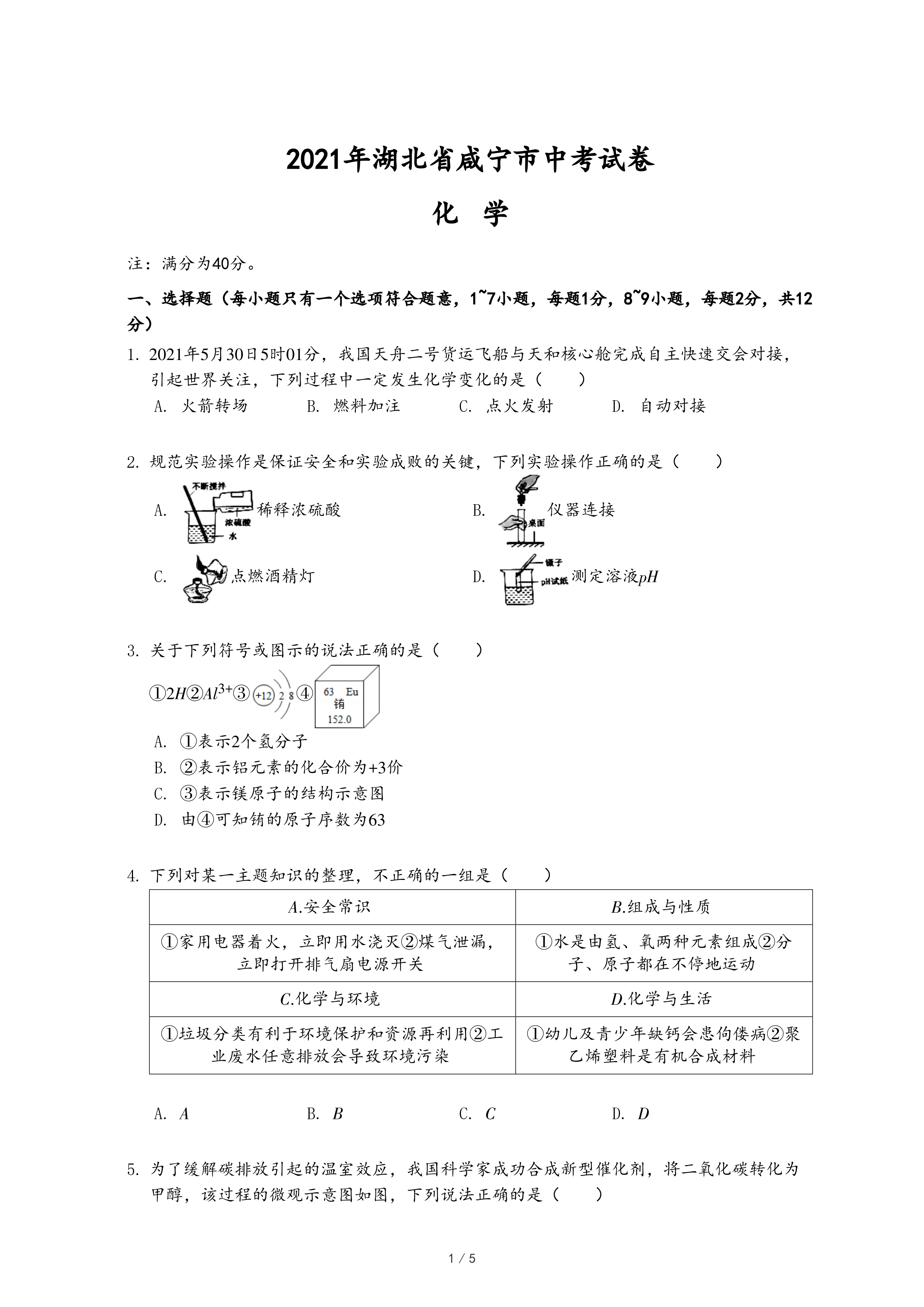
称取干燥的白色不溶物36.8g,充分加热至不再产生气体,并使分解产生的气体全部被如图2所示装置C和D吸收。
【实验数据】实验后装置C增重3.6g,装置D增重13.2g。
(4)【实验结论】若上述白色不溶物的组成用xMg(OH)
2•yMgCO
3表示,则x:y=
。
(5)【反思评价】实验后,同学们经过讨论交流,发现实验方案可进一步优化,下列优化方案错误的是
(填序号)。
①只称量装置C、D增重的质量,不称量白色不溶物的质量
②去掉装置D,只称量白色不溶物和装置C增重的质量
③去掉装置C,只称量白色不溶物和装置D增重的质量



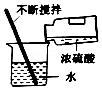 稀释浓硫酸
稀释浓硫酸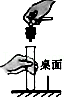 仪器连接
仪器连接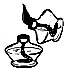 点燃酒精灯
点燃酒精灯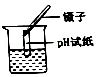 测定溶液pH
测定溶液pH ④
④