14.某化学兴趣小组进行锌与硫酸溶液反应的实验,并用大气球收集产生的气体。同学们在收集过程中闻到一股刺激性气味,同时发现充满气体的气球在空气中有些下沉,有些悬浮,还有些上浮。大家对这些现象很感兴趣,进行了相关探究活动。
【提出问题】锌和硫酸溶液反应后生成的气体是什么?
【查阅资料】
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气体和水。
(2)SO
2有刺激性气味,易溶于水,能使品红溶液褪色。SO
2和CO
2化学性质相似,都能和NaOH等碱溶液反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的平均相对分子质量为29。
【提出猜想】
猜想一:气球内的气体为SO
2;
猜想二:气球内的气体为SO
2和H
2;
猜想三:气球内的气体为H
2。
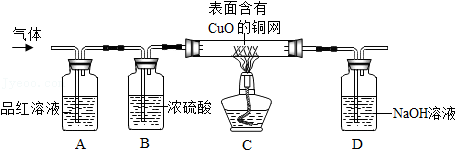
【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同气球内的气体进行探究。
(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是
。
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是
。
(3)乙同学观察到
,说明猜想二正确。
丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
【实验结论】通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
【拓展反思】
(4)下列物质中不能由金属和稀硫酸反应直接得到的是
。
A、Al
2(SO
4)
3B、Fe
2(SO
4)
3C、MgSO
4D、ZnSO
4(5)浓硫酸与铜在加热的条件下反应生成硫酸铜、二氧化硫气体和水,而稀硫酸与铜即使加热也不能反应。这说明:某溶液的化学性质除了与溶质的性质有关外,还可能与下列中的
有关(填序号)。
A.溶质的质量分数
B.溶液的质量
C.溶液的体积
D.溶质的相对分子质量
(6)锌与铜分别和浓硫酸在一定条件下都可以反应产生二氧化硫,若选择铜与浓硫酸在加热的条件下反应制取二氧化硫气体,其优点是
。
(7)实验中下沉的气球内一定含有的气体是
。(填化学式)



 倾倒液体
倾倒液体 测溶液的pH
测溶液的pH 读取液体体积
读取液体体积 检验蜡烛燃烧有水生成
检验蜡烛燃烧有水生成