23.某化学兴趣小组的同学在做酸碱中和反应的实验时,向盛有氢氧化钙溶液的烧杯中加入一定量的稀盐酸后,忘了滴加酚酞溶液不知道盐酸是否过量。于是他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分进行了探究。
【提出问题】该烧杯内溶液中的溶质是什么?
(1)【猜想与假设】猜想一:CaCl
2;
猜想二:
;
猜想三:CaCl
2和Ca(OH)
2;
猜想四:CaCl
2、HCl和Ca(OH)
2。
(2)【交流讨论】同学们讨论后一致认为猜想四不合理,理由是
(用化学方程式表示)。
【实验设计】同学们设计了如下实验方案,请完成下列表格。
| | 操作步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | (3)________正确 |
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入碳酸钠溶液至过量 | (4)________ | 猜想二正确 |
(3)
正确;
(4)
。
(5)【反思交流】方案一不能证明猜想一是否正确,理由是
;若要完善此方案,可将酚酞溶液换成
。
【拓展与应用】
(6)实验证明猜想二正确,要使烧杯内溶液的溶质只含有CaCl
2,需要除去杂质,其中一种方法是向烧杯中加入过量的
,然后过滤。
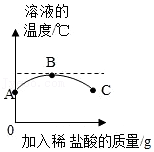
(7)室温下,将稀盐酸慢慢滴入装有氢氧化钙溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液的温度随加入稀盐酸的质量而变化的曲线如图所示。
①由图可知,盐酸与氢氧化钙溶液发生的中和反应是
(填“吸热”、“放热”或“无热量变化”)反应。
②B点对应溶液中的溶质是
(填化学式)。
③B到C的过程中溶液的pH逐渐
(填“增大”、“减小”或“无变化”)。



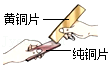
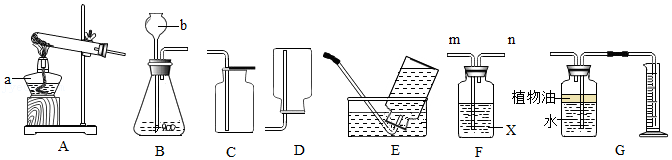
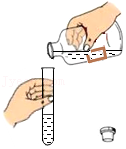 倾倒液体
倾倒液体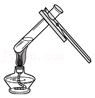 加热液体
加热液体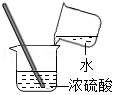 稀释浓硫酸
稀释浓硫酸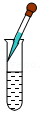 滴加液体
滴加液体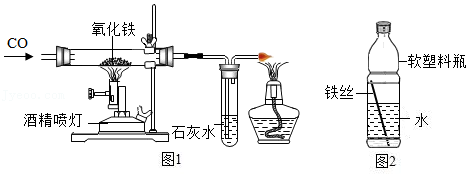
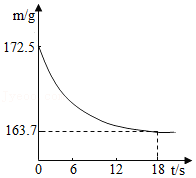
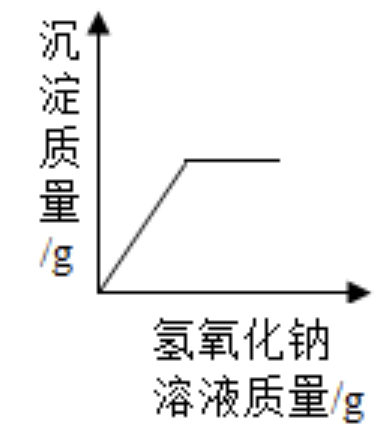 在稀硫酸和硫酸铁的混合溶液中滴加氢氧化钠溶液直至过量
在稀硫酸和硫酸铁的混合溶液中滴加氢氧化钠溶液直至过量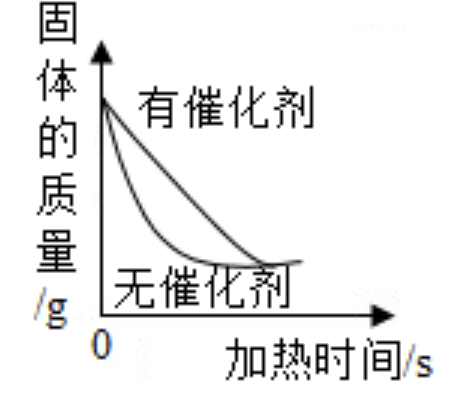 用两份等质量的氯酸钾固体制氧气,其中一份加入少量催化剂
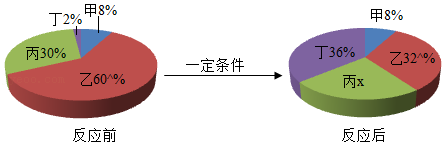
用两份等质量的氯酸钾固体制氧气,其中一份加入少量催化剂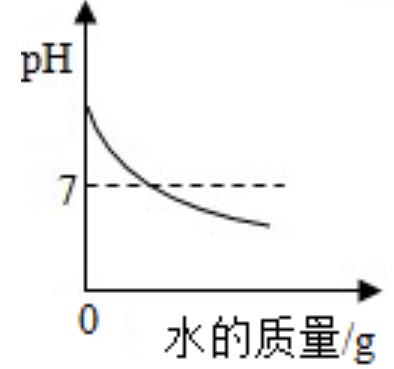 向一定量的氢氧化钠溶液中不断加水
向一定量的氢氧化钠溶液中不断加水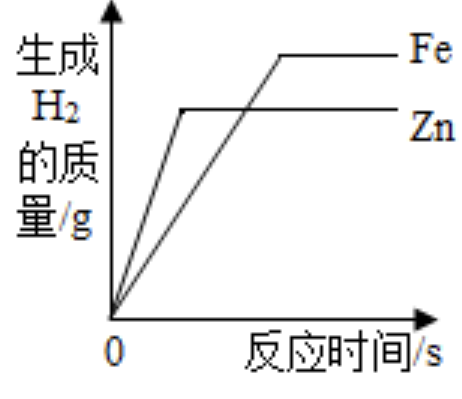 常温下,相同质量的铁和锌分别与质量分数相同的足量稀盐酸反应
常温下,相同质量的铁和锌分别与质量分数相同的足量稀盐酸反应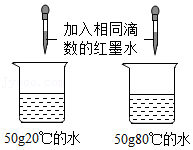

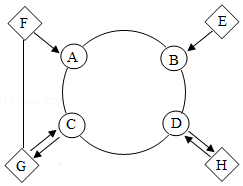
 ”表示两端的物质能发生化学反应,“→”表示物质间在一定条件下存在转化关系,部分反应物生成物及反应条件已略去)。D的溶液呈蓝色常用来配制波尔多液;A是胃酸的主要成分;E是赤铁矿的主要成分;G俗称苏打;C与D反应生成H;F与G发生反应时有气体生成。请回答:
”表示两端的物质能发生化学反应,“→”表示物质间在一定条件下存在转化关系,部分反应物生成物及反应条件已略去)。D的溶液呈蓝色常用来配制波尔多液;A是胃酸的主要成分;E是赤铁矿的主要成分;G俗称苏打;C与D反应生成H;F与G发生反应时有气体生成。请回答: