29.某化学兴趣小组用石灰石(含杂质SiO
2、CaO,还可能含有少量的Fe
2O
3)与足量的稀盐酸制备二氧化碳气体,实验结束后对废液中的溶质成分进行探究(溶解于水中的气体成分忽略不计)。
【提出问题】废液中的溶质含有哪些物质?
【查阅资料】①SiO
2不溶于水,且不与稀盐酸反应;②FeCl
3溶液遇到硫氰化钾(KSCN)溶液能够很灵敏的显现出红色;③FeCl
3只能在较强的酸性溶液中存在,若pH>3.8时,FeCl
3会完全与水发生反应生成Fe(OH)
3沉淀;④CaCl
2溶液为中性。
【假设猜想】
(1)该小组同学一致认为废液中一定含有CaCl
2,用化学方程式表示其原因是
。
(2)结合以上资料,该小组同学作出以下四种的猜想:
猜想1:溶质只有 CaCl
2猜想2:溶质只有CaCl
2和HCl
猜想3:溶质只有 CaCl
2和FeCl
3猜想4:溶质有
。
经讨论,一致认为以上猜想有一种是错误的,该错误猜想是
,理由是
。
(3)【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤1:取少量过滤后的废液于试管中,滴加溶液 。 | 溶液没有变红 | 废液的溶质中不含 FeCl3 |
| 步骤2:另取少量过滤后的废液于试管中,加入过量的Na2CO3溶液。 | 。 | 猜想2成立 |
【反思评价】
(4)上述步骤2中,有同学提出可以通过检测废液的pH来判断是否含有HCl,你认为该方案是否合理,理由是
。
(5)还有同学认为根据实验结论,实验结束后可回收利用CaCl
2溶液,其正确的操作是:向废液中加入过量的
(用化学式),过滤。
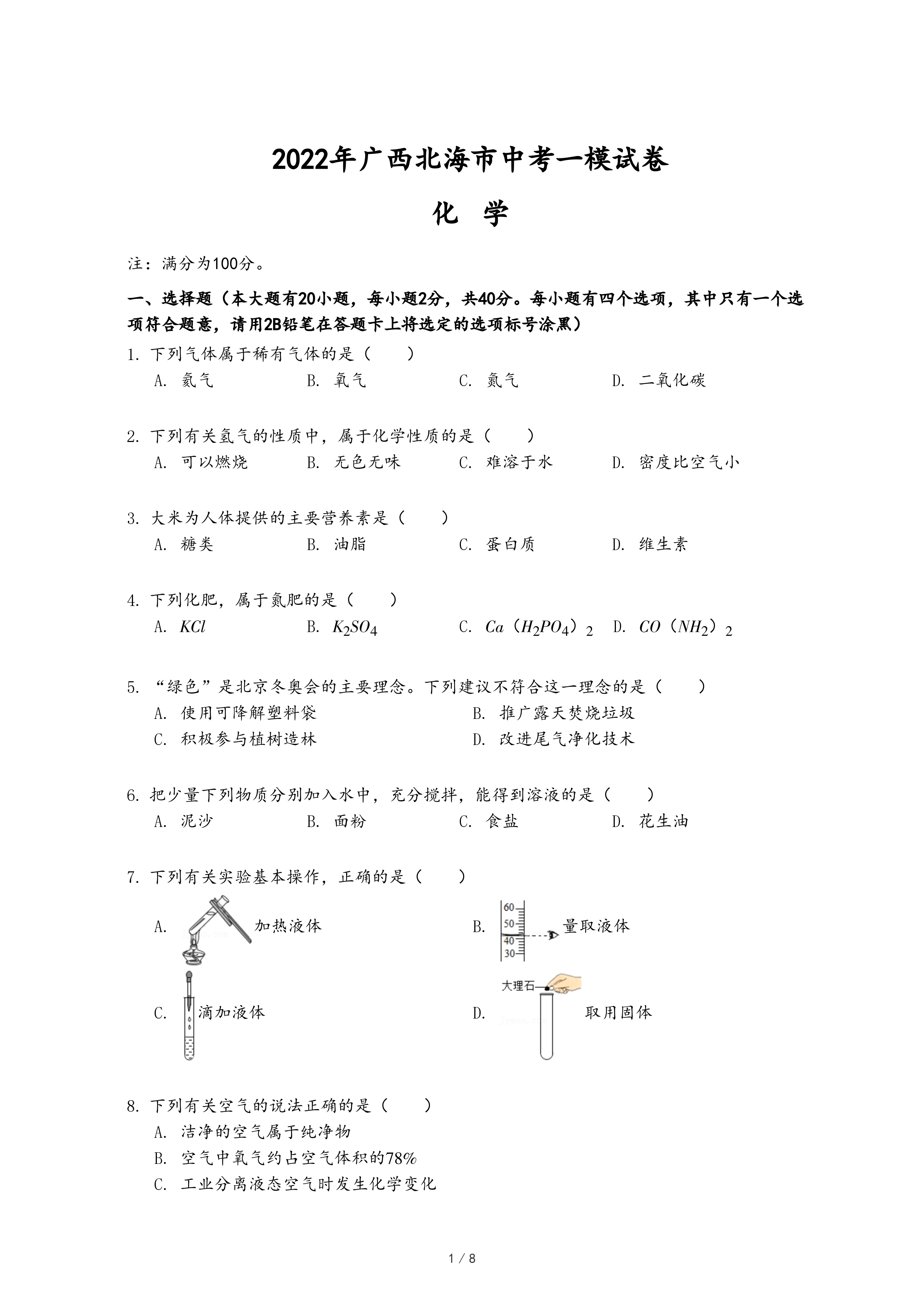



 加热液体
加热液体 量取液体
量取液体 滴加液体
滴加液体 取用固体
取用固体


 表示的粒子在化学反应中易 (填“得”或“失”)电子,形成的离子符号为 。
表示的粒子在化学反应中易 (填“得”或“失”)电子,形成的离子符号为 。




