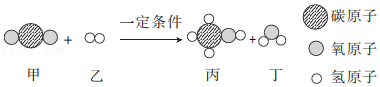
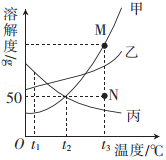
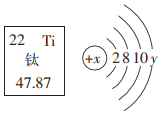
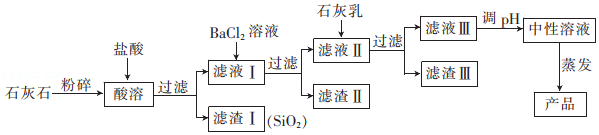
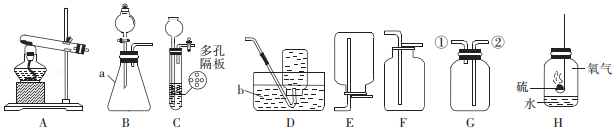
19.同学们在帮老师整理实验室时发现一瓶装有金属钠的试剂瓶,观察到金属钠存放在煤油中,同学们对金属钠非常感兴趣,在老师的帮助下,对以下问题进行了实验探究。
【查阅资料】金属钠的化学性质活泼,常温下极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。
探究一:用小刀切一颗绿豆大小的金属钠投入装有少量蒸馏水的烧杯中,观察到金属钠漂浮于水面上并四处游动,伴有嘶嘶的响声及白雾,金属钠慢慢地熔化成一个光亮的小球,产生一种具有可燃性的单质气体,用手触摸烧杯外壁,感觉发热,反应结束后往烧杯中滴入无色酚酞溶液,溶液变红。
(1)【实验分析】金属钠能与水反应。请写出反应的化学方程式:
。
(2)【交流与反思】金属钠保存在煤油中的原因是
。
探究二:【提出问题】金属钠能否与二氧化碳反应?
【进行实验】按如图装置进行实验,向盛有金属钠的硬质玻璃管中通入纯净、干燥的CO
2,当观察到澄清石灰水中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入二氧化碳,钠剧烈燃烧,产生白烟,燃烧结束后玻璃管中有黑色颗粒和白色固体生成。
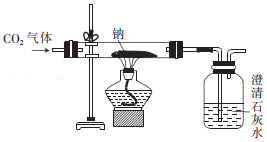
【问题讨论】
(3)点燃酒精灯前,要先向玻璃管中通一会儿二氧化碳,其目的是
。
实验中生成的黑色颗粒是碳,那白色固体可能是什么呢?
(4)【继续探究】同学们围绕白色物质可能是什么进行了如下猜想:
猜想①:氧化钠;
猜想②:碳酸钠;
猜想③:氧化钠和碳酸钠的混合物;
猜想④:氢氧化钠。
大家讨论后一致认为猜想④是错误的,理由是
。
【实验设计】同学们设计了以下探究方案:
方案1:取该样品少量于试管中,加入适量的水,振荡,过滤,向滤液中加入无色酚酞溶液,观察到溶液变成红色,则白色固体中一定有氧化钠。
方案2:取该样品少量于试管中,滴加足量稀盐酸,溶液中有气泡冒出。则白色固体中一定有碳酸钠。
方案3:取该样品少量于试管中,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液,出现白色沉淀,过滤,再向滤液中滴加无色酚酞溶液,无明显现象。
(5)【实验分析】小红认为方案1的结论不合理,原因是
。方案3中加入过量CaCl
2溶液的目的是
。根据以上探究,你认为猜想
正确。
【实验结论】金属钠能与二氧化碳反应。
(6)【交流与反思】结合金属钠部分性质的探究,小金对燃烧的条件有了新的认识,燃烧
(选填“一定”或“不一定”)需要氧气。








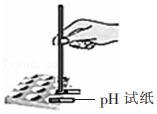 用pH试纸测定溶液的酸碱度
用pH试纸测定溶液的酸碱度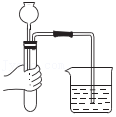 检查气密性
检查气密性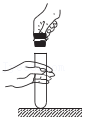 塞紧橡胶塞
塞紧橡胶塞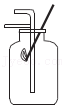 CO2验满
CO2验满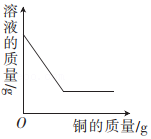 向一定质量的硝酸银溶液中加入铜粉
向一定质量的硝酸银溶液中加入铜粉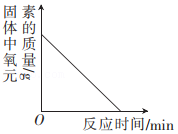 一定条件下氧化铜和炭粉恰好完全反应
一定条件下氧化铜和炭粉恰好完全反应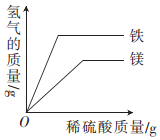 等质量的镁和铁分别与足量的稀硫酸反应
等质量的镁和铁分别与足量的稀硫酸反应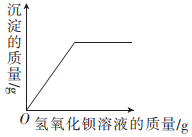 向一定量盐酸和硫酸钠的混合溶液中滴加氢氧化钡溶液
向一定量盐酸和硫酸钠的混合溶液中滴加氢氧化钡溶液