







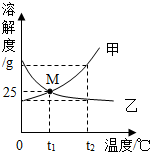
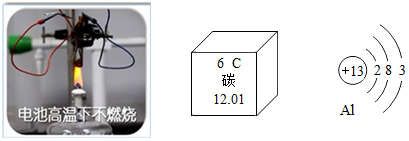
| 选项 | 操作 | 现象 | 结论 |
| A | 取50mL水和50mL酒精混合 | 总体积小于100mL | 分子间存在间隔 |
| B | 取柠檬汁样品滴加几滴石蕊试液 | 溶液变蓝 | 柠檬汁呈酸性 |
| C | 在含少量盐酸的CaCl2溶液中加入适量纯碱 | 产生气泡 | 除去了CaCl2溶液中的杂质 |
| D | 在CuSO4溶液中插入锌片和铁片 | 锌片和铁片表面均出现红色固体 | 金属的活动性锌>铁>铜 |
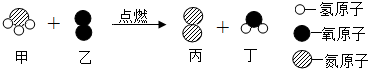

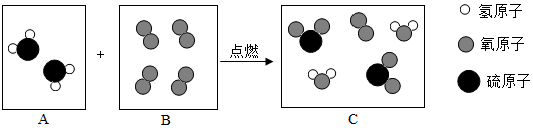

| 通电 |
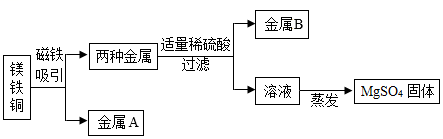
| 实验步骤 | 实验现象 | 实验结论 |
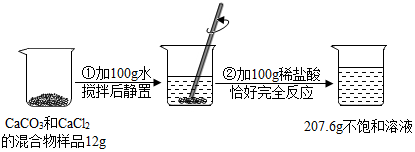
| 步骤①:取少量固体样品溶于水。 | 固体溶解,溶液温度明显上升 | 猜想正确 |
| 步骤②:待步骤①中溶液冷却后,向溶液中滴加过量 。 | 开始无明显变化,后产生气泡 | |
| 步骤③:向步骤②所得溶液中滴加 溶液。 | 产生白色沉淀 |