19.化学兴趣小组同学将镁条放入盛有NH
4Cl溶液的试管中,微热后发现产生无色气体,还生成白色沉淀。
【提出问题】问题一:气体有什么成分?问题二:白色沉淀有什么成分?
【查阅资料】①氯化铵溶液显酸性。
②无水硫酸铜吸水变蓝。
③Mg(OH)
2受热分解成MgO和H
2O:碱式氯化镁【Mg(OH)Cl】不溶于水,受热分解生成MgO和HCl气体。
实验一:探究气体的成分
【作出猜想】气体可能含有NH
3,小组同学根据氯化铵溶液显酸性,猜测气体中也可能含有
。
【实验探究】甲同学用湿润的红色石蕊试纸靠近试管口,观察到试纸
,证明气体中含有NH
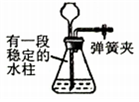
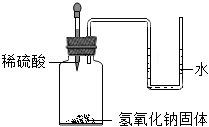
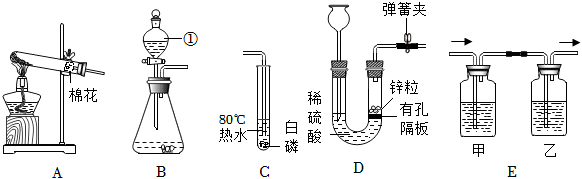
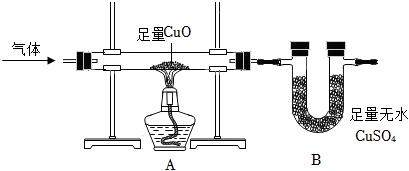
3。乙同学收集了部分气体,通过足量浓硫酸后,利用如图装置进行实验,证明另一种气体存在。硬质玻璃管中反应的方程式为
,加热前先通入气体,目的为
。
实验二:探究白色沉淀的成分
【作出猜想】白色沉淀可能含Mg、Mg(OH)
2或Mg(OH)Cl中的一种或多种
【实验探究】丙同学取部分白色沉淀于试管中,加入
(填物质名称),观察到沉淀消失且没有气泡产生,则白色沉淀中不含Mg。
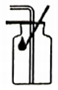
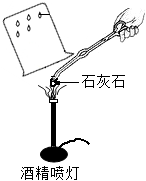
丙同学另取6g白色沉淀,置于如图装置玻璃管中,充分加热后,玻璃管中剩余固体质量为4g。通过推算可知白色沉淀的成分为
。
【拓展延伸】碱式盐在生活中应用广泛。碱式氯化铝【Al
2(OH)Cl
5】是一种高效净水剂。已知碱式氯化铝与盐酸发生反应生成氯化铝和常见的溶剂,则此反应的方程式为
。