




| A.物质的分类 | B.物质的鉴别 |
| ①合金:黄铜,氧化铜 ②复合肥:尿素,硝酸钾 ③碱:纯碱,熟石灰 | ①用灼烧闻气味的方法鉴别羊毛和棉纤维 ②用稀盐酸区分CuO粉末和碳粉 ③用水鉴别氯化钠固体和硝酸铵固体 |
| C.物质的用途 | D.物质的性质 |
| ①明矾常用于除去水中的颜色和异味 ②干冰可用于人工降雨 ③一氧化碳可用于冶炼金属 | ①自来水可以养鱼说明氧气易溶于水 ②“真金不怕火炼”,说明金的熔点高 ③铁用来做锅说明铁具有导热性 |
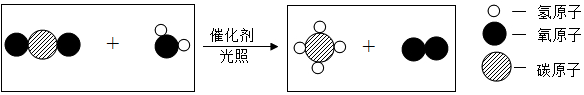
| 选项 | 实验目的 | 方案 |
| A | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐溶解、过滤、蒸发结晶 |
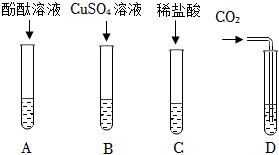
| C | 探究Mg、Ag、Cu金属的活动性顺序 | 将两根光亮的镁条分别伸入硫酸铜溶液和硝酸银溶液中,观察。 |
| D | 测定空气中氧气的含量 | 将白磷放入有刻度的玻璃管(一端封闭,另一端可移动活塞,记录初始读数),水浴使白磷燃烧,等冷却后再次读数,计算。 |
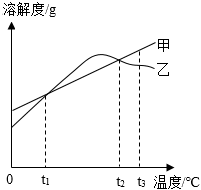
| 温度℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | |
| 溶解度/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 | 52.9 | 52.2 |
| KCl | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 | 54.0 | |