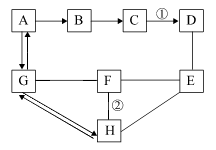
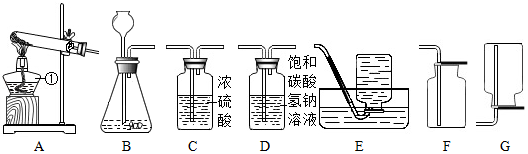
22.化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
【提出问题】瓶口白色固体的成分是什么?
【查找资料】(1)玻璃中含有二氧化硅(SiO
2),试剂瓶身经抛光处理,不易反应,而瓶口和玻璃塞上的磨砂将二氧化硅裸露出来;
(2)二氧化硅能与氢氧化钠溶液反应,SiO
2+2NaOH=Na
2SiO
3+H
2O;
(3)硅酸钠(Na
2SiO
3)是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性;硅酸钠溶液能与强酸反应,如:Na
2SiO
3+2HCl=2NaCl+H
2SiO
3↓(白色);
硅酸钠溶液能与氯化钙溶液反应:Na
2SiO
3+CaCl
2=2NaCl+CaSiO
3↓(白色)。
【作出猜想】白色固体的成分是:
Ⅰ.硅酸钠;
Ⅱ.硅酸钠和碳酸钠;
Ⅲ.硅酸钠、碳酸钠和氢氧化钠
【实验探究】取一定量白色固体溶于适量水中形成样品溶液,分组进行如下实验并相互评价:
| | 实验操作 | 实验现象 | 结论与评价 |
| 第1组 | 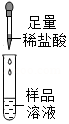 | 有气泡冒出且产生白色沉淀 | 同学们认为猜想① 不成立;写出生成气体的反应化学方程式:② |
| 第2组 | 第一步 |  | 产生白色沉淀 | 第1组同学认为:此步骤还不能准确判断出原固体的成分。 |
| 第二部 |  | ③ | 大家一致认为:猜想II成立。 |
【反思交流】
(1)有同学认为,第2组实验中不能用氢氧化钙溶液代替氯化钙溶液,理由是:④
;
(2)氢氧化钠溶液必须密封保存,且试剂瓶只能用橡胶塞。
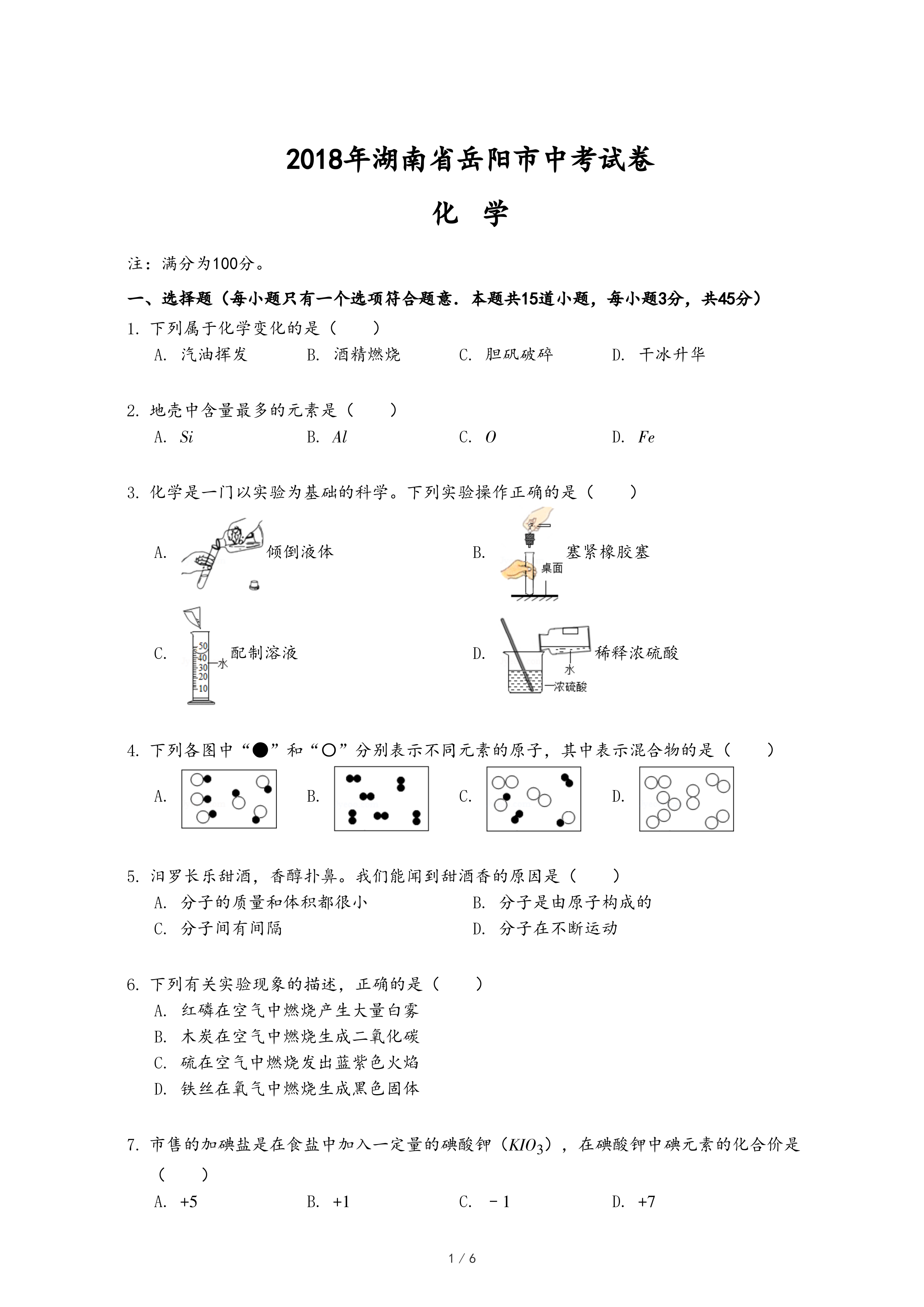













 倾倒液体
倾倒液体 塞紧橡胶塞
塞紧橡胶塞 配制溶液
配制溶液 稀释浓硫酸
稀释浓硫酸


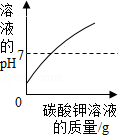 向一定量的盐酸和氯化钡的混合溶液中,逐渐滴加碳酸钾溶液至过量
向一定量的盐酸和氯化钡的混合溶液中,逐渐滴加碳酸钾溶液至过量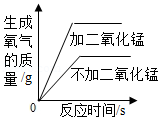 加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加入二氧化锰
加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加入二氧化锰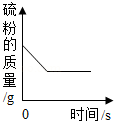 一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应
一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应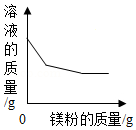 向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量
向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量