28.〖科普阅读理解〗
阅读下列科普短文。
莲藕是一种营养价值很高的食品。新鲜的莲藕中含有丰富的营养物质。
新鲜莲藕中主要营养物质的含量(每100 g)
| 淀粉/g | 蛋白质/g | 脂肪/g | 维生素/mg | 钙/mg | 磷/mg | 铁/mg |
| 10~20 | 1~2 | 0.2 | 25~55 | 39 | 58 | 1.4 |
莲藕经加工后可制成多种食品,如藕粉、藕片糖及藕脯等。藕粉加工工艺流程如下:
挑选→清洗→整作→轧浆→过滤→清漂(沉淀)→抽燥→晒干→捻碎→成品→贮存
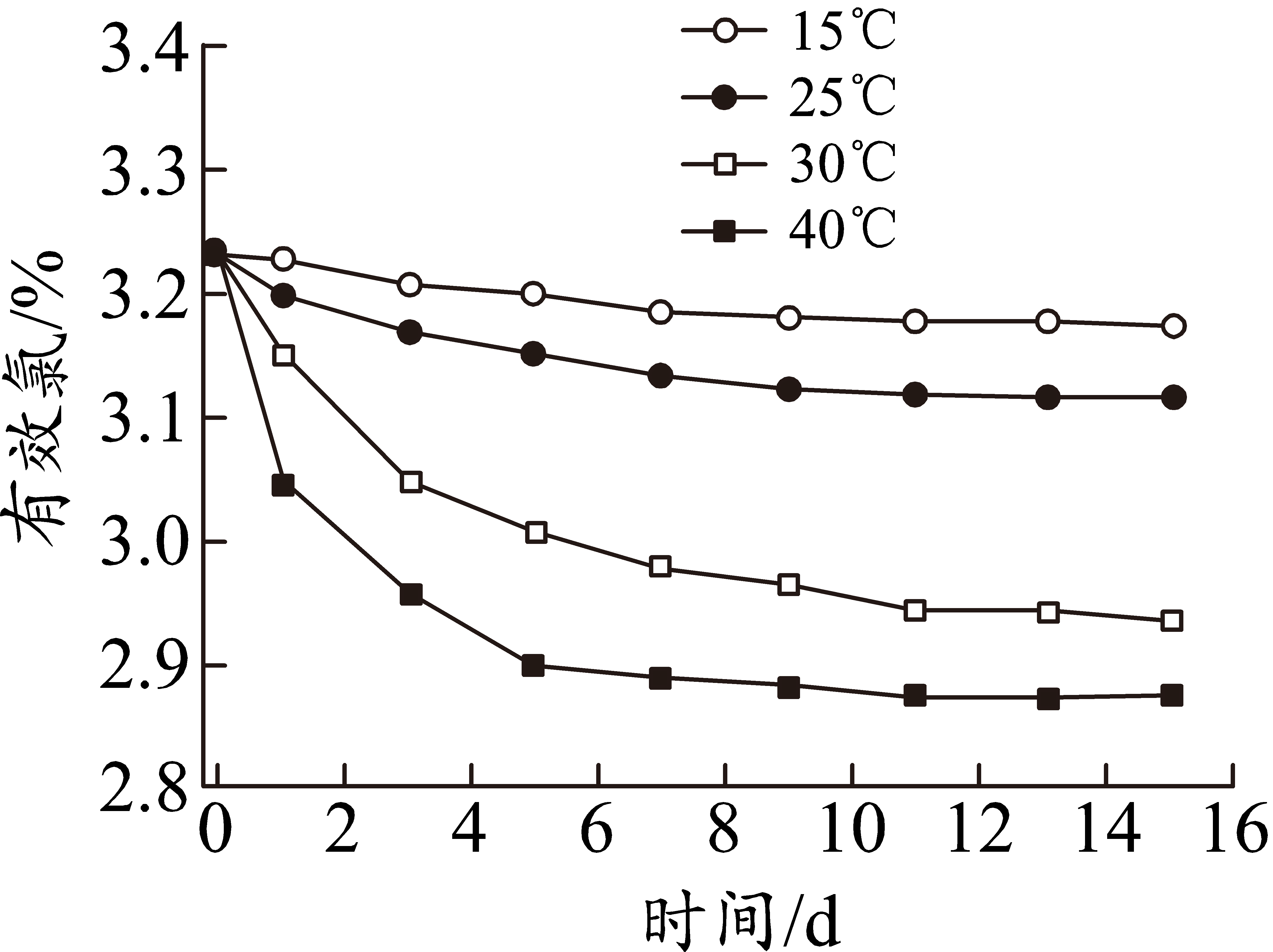
某些加工工艺中,将捻碎后的藕粉再进行超微粉碎。超微粉碎后,藕粉中的淀粉结构被破坏,促进其与水分子的结合,使藕粉具有更好的膨胀度,能快速溶解。下图为不同温度下捻碎和超微粉碎后藕粉膨胀度的比较。
此外,纯藕粉与空气接触后极易氧化,颜色由白色变为微红色,但不妨碍食用。
除食用外,莲藕还有很好的药用价值,具有补血益气、开胃健脾的功效。
依据文章内容回答下列问题。
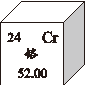
(1)表中含量最高的营养素是
;“钙”是指
(填“原子”或“元素”)。
(2)依图判断,下列说法正确的是
(填序号,下同)。
A.实验做了2组,每组选定9个温度
B.实验范围内,两种藕粉的膨胀度均随温度升高而升高
C.实验范围内,温度越高,两种藕粉的膨胀度差异越大
(3)藕粉在保存过程中会出现微红色,其原因是
。
(4)下列说法正确的是
。
A.超微粉碎会破坏藕粉中的淀粉结构
B.超微粉碎后的藕粉可制成速溶食品
C.莲藕具有很好的药用价值