


















| +3 |
| Al |
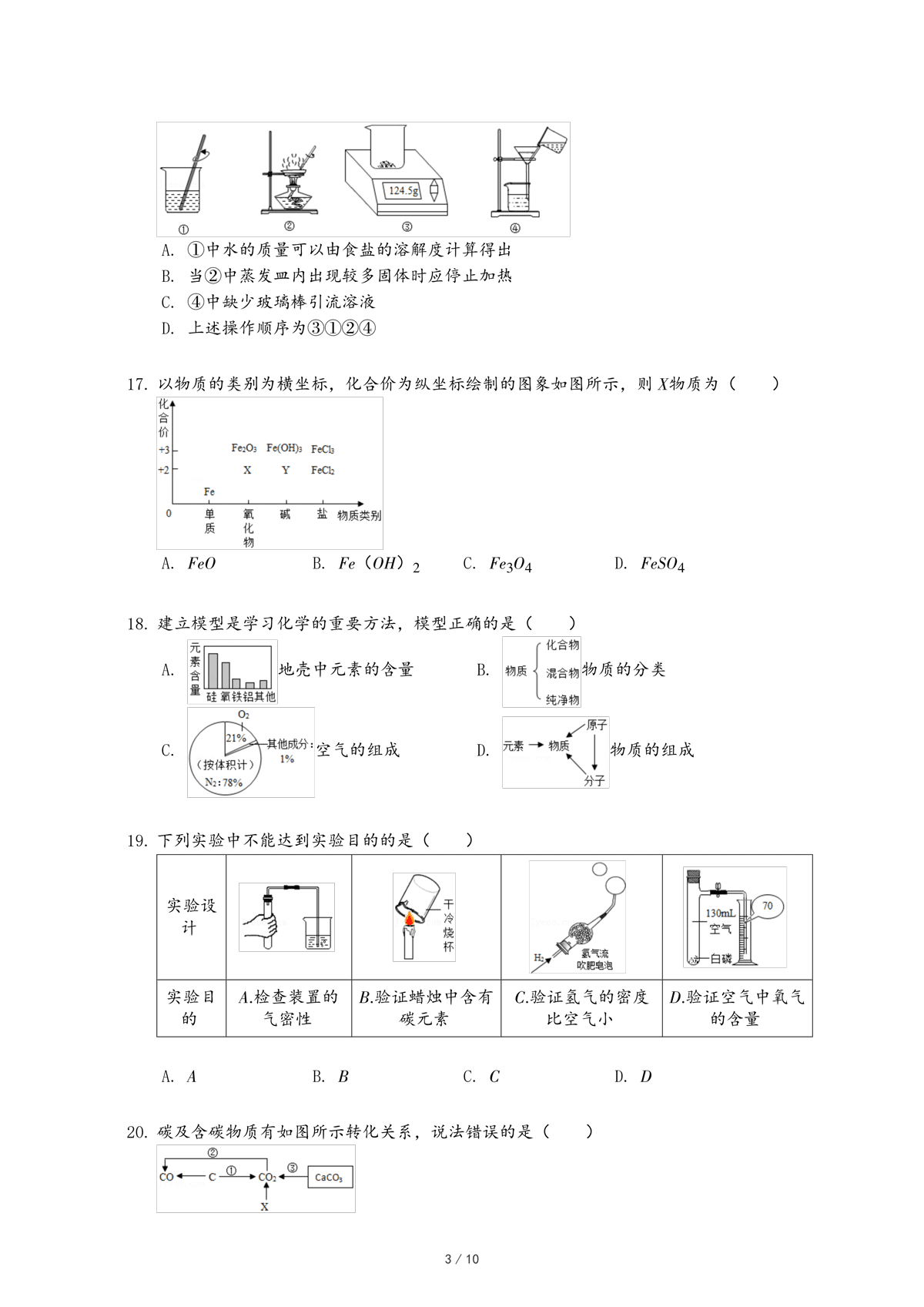
 滴加液体
滴加液体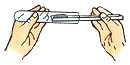 取用固体
取用固体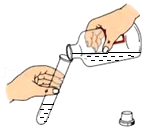 取用液体
取用液体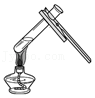 加热液体
加热液体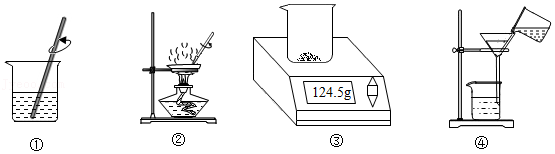
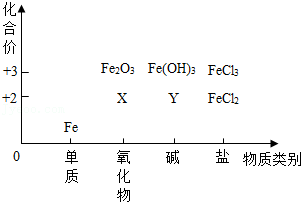
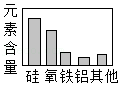 地壳中元素的含量
地壳中元素的含量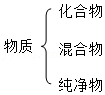 物质的分类
物质的分类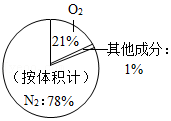 空气的组成
空气的组成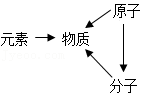 物质的组成
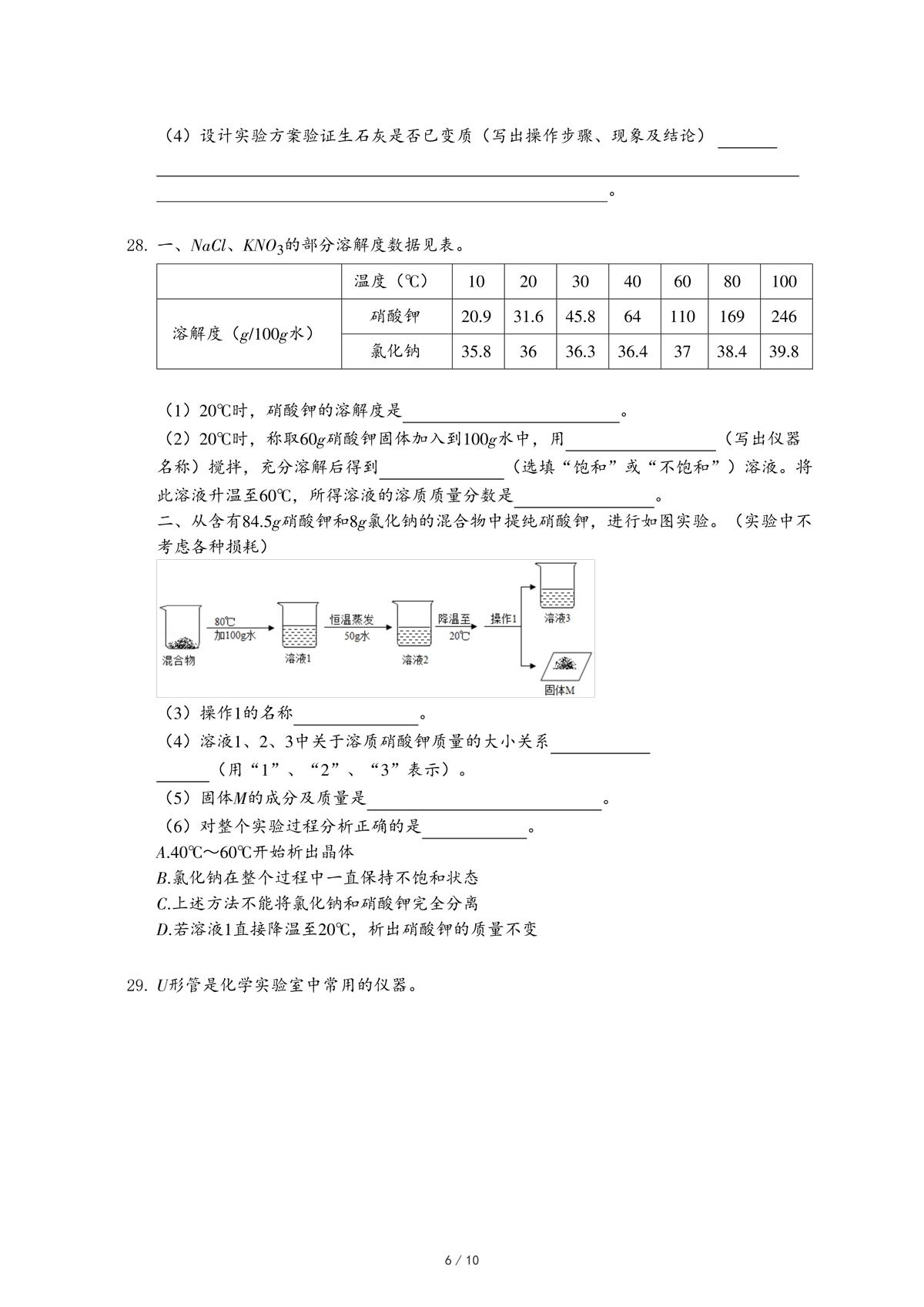
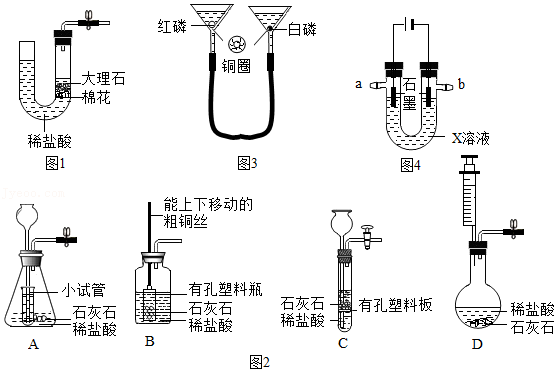
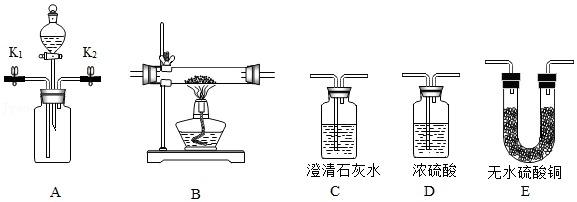
物质的组成| 实验设计 | 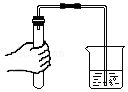 | 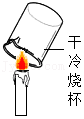 | 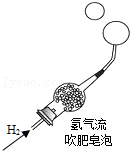 | 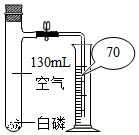 |
| 实验目的 | A.检查装置的气密性 | B.验证蜡烛中含有碳元素 | C.验证氢气的密度比空气小 | D.验证空气中氧气的含量 |
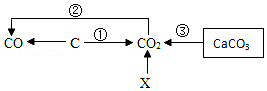
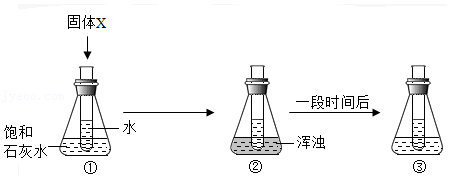
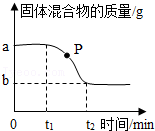
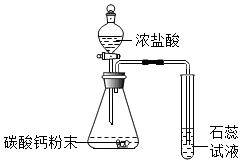
| 紫外线 |
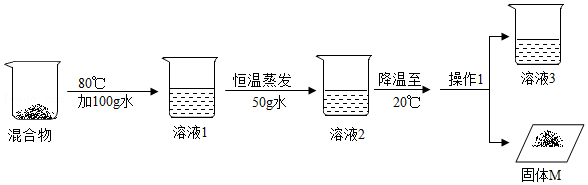
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | 硝酸钾 | 20.9 | 31.6 | 45.8 | 64 | 110 | 169 | 246 |
| 氯化钠 | 35.8 | 36 | 36.3 | 36.4 | 37 | 38.4 | 39.8 |
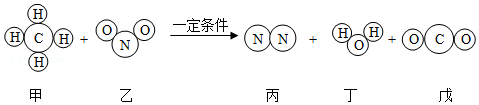
| 通电 |
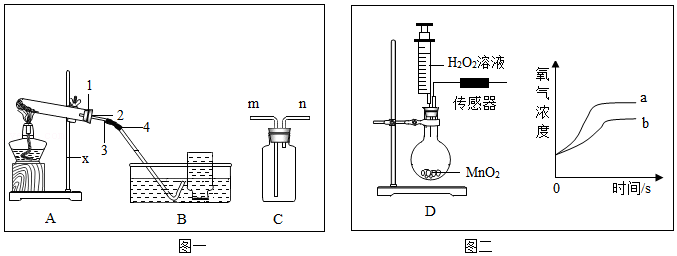
| 试验编号 | H2O2的质量分数(%) | H2O2溶液的体积(mL) | 对应曲线 |
| Ⅰ | 3.4 | 10.0 | a |
| Ⅱ | 2.4 | ________ | b |
| Ⅲ | 1.7 | 10.0 | c(待绘制) |
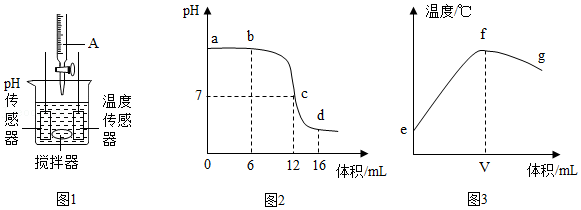
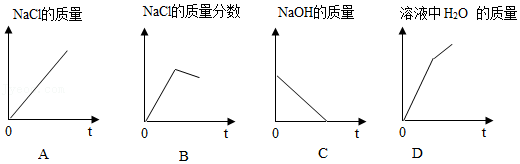
| △ |