12.碳酸锶(SrCO
3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO
3,少量MgCO
3、CaCO
3、BaCO
3等)制备高纯碳酸锶的工艺流程如图:
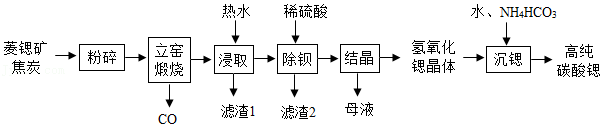
(查阅资料)①不溶性碳酸盐高温下可以分解,生成金属氧化物和CO
2气体。可溶性碳酸盐高温不分解。
②可溶性碱(如KOH)中金属元素(K)形成的氧化物(K
2O)才能与水反应生成对应的碱(KOH),反之,不溶性碱[如Cu(OH)
2]中金属元素(Cu)形成的氧化物(CuO)不能与水反应。
③金属锶:化学性质非常活泼,可直接与水反应生成氢氧化锶和氢气。
④氢氧化锶在水中的溶解度数据如表:
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
请回答以下问题:
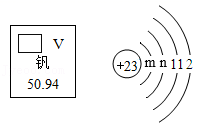
(1)碳酸锶(SrCO
3)中锶的化合价为
,氢氧化锶的化学式为
。
(2)菱锶矿、焦炭混合粉碎的目的是
。
(3)立窑煅烧中将得到单质锶,请写出得到单质锶的化学方程式
。
(4)请写出杂质BaCO
3在立窑煅烧和浸取两个环节中发生的化学方程式
、
。
(5)“浸取”中用热水浸取而不用冷水的原因是
,滤渣1含有焦炭、Ca(OH)
2和
。
(6)“结晶”采用的是
结晶法,“沉锶”反应中氢氧化锶和NH
4HCO
3发生反应,产物除了碳酸锶外,还有水和一水合氨,请写出该反应的化学方程式
。
(7)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。要制备某种锶铁氧体(化学式为SrO•6Fe
2O
3,相对分子质量为1064)5.32t,理论上至少需要NH
4HCO
3的质量为多少吨?(写出计算过程)。














 食醋(3~4)
食醋(3~4) 海水(8~9)
海水(8~9) 肥皂水(10~11)
肥皂水(10~11) 洗涤剂(12~13)
洗涤剂(12~13) 红烧鱼
红烧鱼 炸鸡翅
炸鸡翅 米饭
米饭 炒黄瓜片
炒黄瓜片 证明分子在不停地运动
证明分子在不停地运动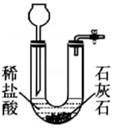 控制反应的发生与停止
控制反应的发生与停止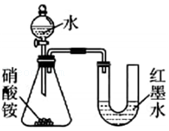 证明硝酸铵溶解时吸热
证明硝酸铵溶解时吸热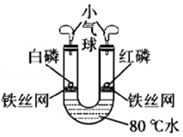 探究燃烧需要氧气
探究燃烧需要氧气