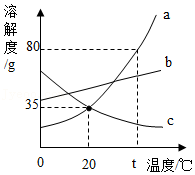
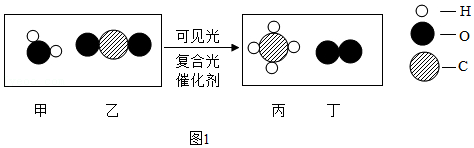
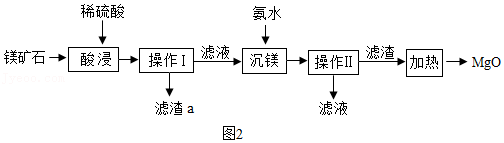
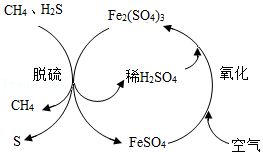
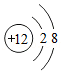16.工业铁红主要成分是Fe
2O
3,还含有少量的FeO、Fe
3O
4。
【查阅资料】
1.草酸晶体(H
2C
2O
4•3H
2O)在浓硫酸作用下受热分解,化学方程式为:H
2C
2O
4•3H
2O
CO
2↑+CO↑+4H
2O。
2.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
3.铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
【实验、分析讨论】为测定铁红中铁的质量分数,小组同学进行如图实验(气密性良好)。
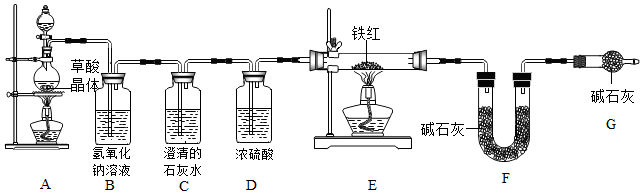
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,所以需依次经过B、C、D装置,写出装置B中发生的方程式为
;装置C的作用是
。
(2)写出E装置中所发生反应的一个化学方程式
。
(3)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则
<m<
。
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是
。
【实验反思】
(4)如果缺少装置G(不考虑其他因素),则测得样品中铁的质量分数会
(选填“偏小”“不变”或“偏大”)。
该实验装置需加装尾气处理装置防止多余的一氧化碳污染空气。




 闻药品气味
闻药品气味 取用块状物体
取用块状物体 取用盐酸
取用盐酸 稀释浓硫酸
稀释浓硫酸