20.小华同学在探究金属与酸反应时,将铝片、锌片打磨后,分别投入盛有等体积、等浓度稀盐酸的试管中,观察到铝与稀盐酸反应较锌与稀盐酸反应快。
【提出问题】金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
【猜想与假设】a.可能与盐酸的浓度有关;b.可能与反应时的温度有关;c.你的猜想是
。
| 实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 记录的数据 |
| ① | 5% | 30 | |
| ② | 10% | 20 | |
| ③ | 5% | 20 | |
| ④ | 10% | 30 | |
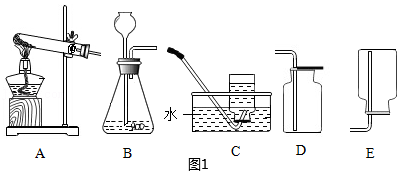
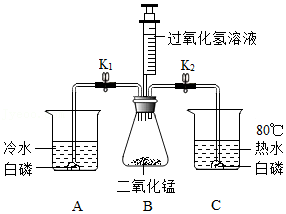
【设计并实验】小明利用图甲所示装置,用不同浓度的盐酸和相同形状的铝片进行如下实验。

【交流讨论】(1)请写出铝与稀盐酸反应的化学方程式
。
(2)实验前小明检查图甲装置的气密性的方法是
。
【分析数据、得出结论】
(3)实验中记录的数据可能是
;对比实验②③可知
对金属与酸反应的速率的影响。
(4)实验表明,四次实验时反应的速率由快到慢依次为④、②、①、③。根据记录的数据分析,如果盐酸浓度为10%,温度为25℃,则所记录数据应该介于
两次实验所记录的数据之间。
(5)小明进行铝与稀盐酸反应时,测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳铝与稀盐酸反应速率的变化规律
。
【拓展延伸】(6)研究小组同学继续探究铝与稀盐酸反应。小组同学用未经打磨的铝和稀盐酸的反应,利用压强和温度传感器测出的反应变化过程,得到如图丙和图丁所示的温度以及气体压强与时间的关系曲线图。

图丁中0﹣50秒的时间温度无明显变化的可能原因是
,CD段气体压力逐渐下降的原因是
。




 厨余垃圾
厨余垃圾 其他垃圾
其他垃圾 有害垃圾
有害垃圾 可回收垃圾
可回收垃圾 衣服晾干
衣服晾干 木柴燃烧
木柴燃烧 西瓜榨汁
西瓜榨汁 冰块融化
冰块融化
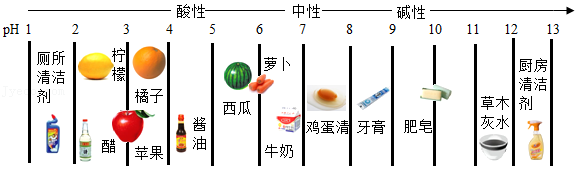
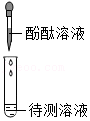 证明待测溶液呈酸性
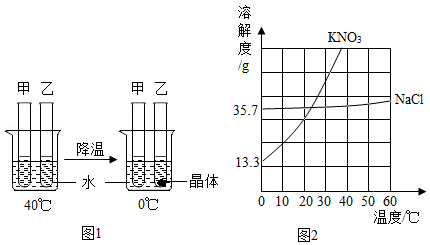
证明待测溶液呈酸性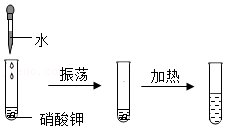 探究硝酸钾溶解度与温度的关系
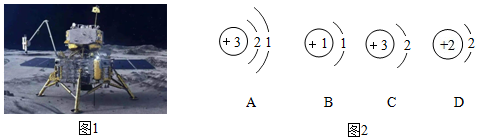
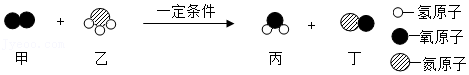
探究硝酸钾溶解度与温度的关系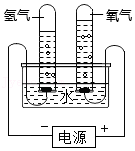 探究水的组成元素
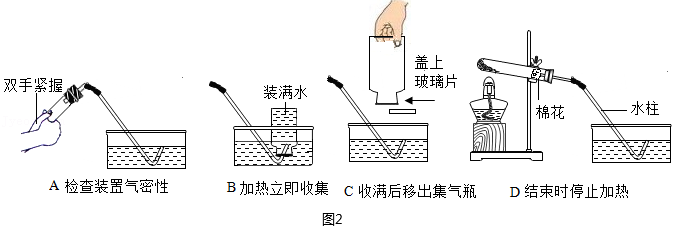
探究水的组成元素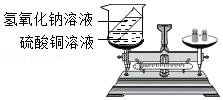 验证质量守恒定律
验证质量守恒定律