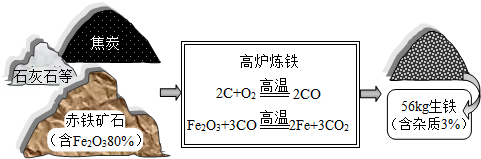
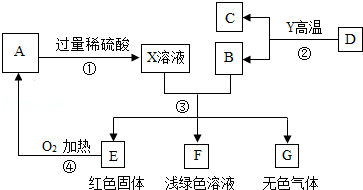
25.小明同学在实验室将镁放入NH
4Cl溶液中,发现有气泡产生。询问老师后得知镁与NH
4Cl溶液反应能生成气体和一种盐。为了确定气体的成分,进行下列实验探究:
探究一:
【查阅资料】①NH
4Cl溶液显酸性;
②NH
3+HCl=NH
4Cl,2NH
3+H
2SO
4=(NH
4)
2SO
4③2NH
3+3CuO
3Cu+N
2+3H
2O
【提出猜想】反应生成的气体可能是HCl、NH
3、H
2中的一种或几种
【探究实验】
(1)用湿润的紫色石蕊试纸检验,试纸不变
色,则该气体中无HCl气体。
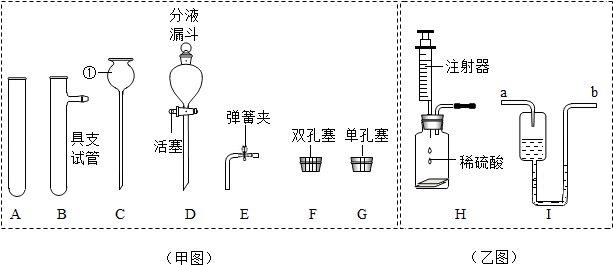
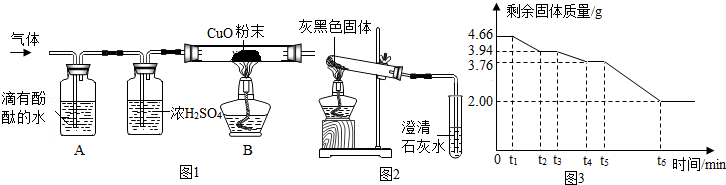
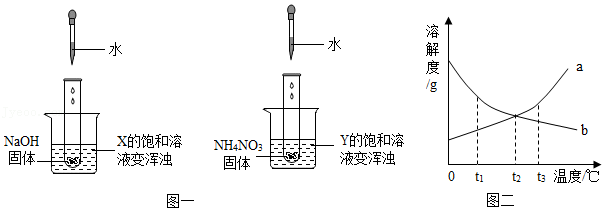
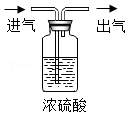
(2)为了探究其它气体是否存在,设计了如图1实验装置。
A中溶液变红色,证明有
气体(填化学式);浓硫酸的作用是
;B中玻璃管内观察到
,说明有氢气。
【实验结论】镁与NH
4Cl溶液反应生成NH
3和H
2,还生成一种盐的化学式是
。
【实验反思】
(1)综合以上信息和实验结论,小林同学认为不需要单独检验HCl气体,就能说明HCl气体不存在。理由是:
。
探究二:镁是一种银白色有金属光泽的金属。但实验时小组同学拿出的镁条却是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
【查阅资料】
(1)Mg(OH)
2:白色固体,难溶于水,受热会分解成氧化镁和水;
(2)MgCO
3:白色固体,微溶于水,受热会分解成氧化镁和二氧化碳;
(3)MgCO
3的热稳定性比Mg(OH)
2的热稳定性更强。
【提出猜想】
小组同学认为该固体不可能是MgO、Mg(OH)
2或MgCO
3,他们的理由是
。
小组同学由铜生锈会产生Cu
2(OH)
2CO
3联想到灰黑色的物质可能是Mg
2(OH)
2CO
3。
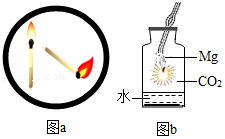
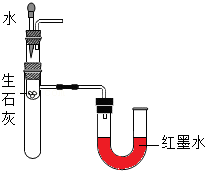
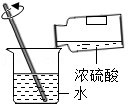
【实验分析】
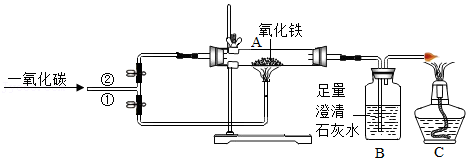
按图2所示装置进行实验,发现试管口有液滴出现;澄清石灰水变浑浊;同时灰黑色固体完全变为白色。若灰黑色固体是Mg
2(OH)
2CO
3,请写出Mg
2(OH)
2CO
3受热分解的化学方程式
。
【组成测定】
工业生产中得到的碱式碳酸镁晶体是4MgCO
3•Mg(OH)
2•zH
2O,为精确测量晶体的组成,小组同学取4.66g该晶体,用热分析仪对固体进行热分解(加热使之逐步分解,首先失去结晶水,最后完全反应),测定剩余固体质量与分解温度之间关系。
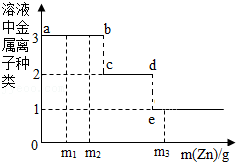
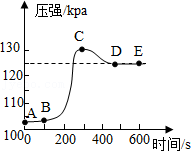
【数据处理】剩余固体质量与加热时间关系如图3所示:
请回答下列问题:
(1)t
4~t
5段固体为
(写化学式)。
(2)根据图中数据推算4MgCO
3•Mg(OH)
2•zH
2O中z的数值是:
。(请写出计算过程)




 验证生石灰与水反应放热
验证生石灰与水反应放热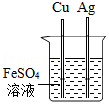 验证Fe、Cu、Ag的金属活动性强弱
验证Fe、Cu、Ag的金属活动性强弱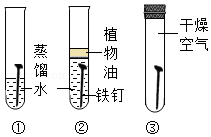 探究铁钉生锈的条件
探究铁钉生锈的条件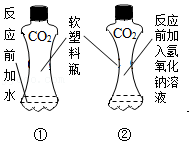 证明CO2与NaOH反应
证明CO2与NaOH反应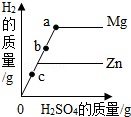




 与
与 的质量之比为17:2
的质量之比为17:2 与
与 的化学计量数之比为2:1
的化学计量数之比为2:1