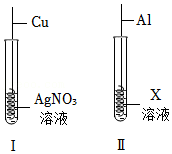
19.学习小组对碱式碳酸铜[化学式为Cu
2 (OH)
2CO
3]的性质进行探究,并进行相关实验。
(1)分析组成
碱式碳酸铜中化合价为﹣1价的原子团是
。
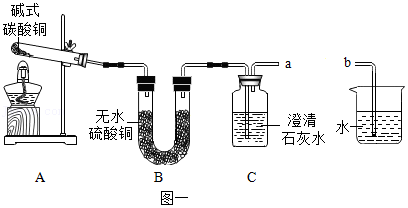
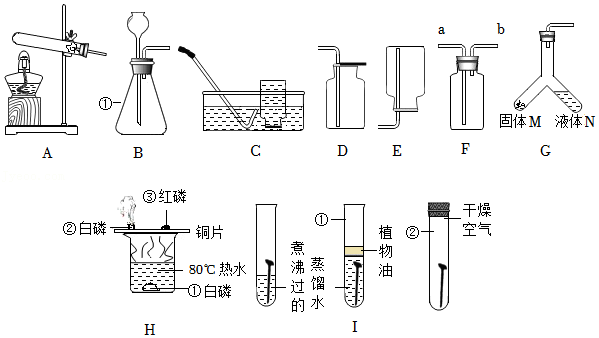
(2)探究分解产物,装置如图一所示(省略夹持仪器):
| 实验步骤 | 现象 | 分析和结论 |
| I.组装装置,连接导管a、b,微热试管。 | ①烧杯中的导管口________。 | 说明整套装置不漏气。 |
| Ⅱ.加入药品和试剂,点燃酒精灯。 | A中固体出现黑色,B中白色固体变蓝,C中石灰水变浑浊。 | ②C中反应的化学方程式为________。
碱式碳酸铜受热分解的产物有CuO、CO2、________。 |
①烧杯中的导管口
。
②C中反应的化学方程式为
。碱式碳酸铜受热分解的产物有CuO、CO
2、
。
用氢气还原装置A中反应后的固体并检验产物,装置如图二所示(F中的无水硫酸铜用于吸收空气中的水蒸气)。
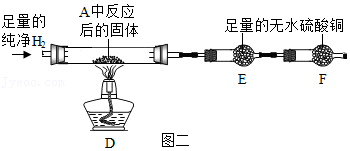
I.D中观察到固体变红。
(3)Ⅱ.实验开始时,若先点燃酒精灯后通氢气,可能导致的后果是
。
(4)Ⅲ.E中观察到白色固体变蓝,发生反应的化学方程式为
,该现象能否证明氢气和氧化铜反应生成了水,理由是
。
学习小组还利用图二装置定量测定水的组成(玻璃管中为纯净氧化铜),并测定了如表的四个数据(单位:g)。
| | 反应前质量 | 反应后质量 |
| 装置D | a | b |
| 装置E | c | d |
(5)利用表格中数据,列式表示水中氢、氧原子的物质的量之比
(不要求化简)。




 雕琢玉石
雕琢玉石 丝线织锦
丝线织锦 葡萄制酒
葡萄制酒 瓷盘破碎
瓷盘破碎 西瓜pH=5.8
西瓜pH=5.8 芒果pH=3.5
芒果pH=3.5 菠萝pH=5.0
菠萝pH=5.0 葡萄pH=4.5
葡萄pH=4.5
 收集氧气
收集氧气 测定盐酸pH
测定盐酸pH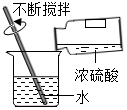 稀释浓硫酸
稀释浓硫酸 探究铁生锈的条件
探究铁生锈的条件