15.小组同学将几枚生锈的铁钉放入盛有足量可乐饮料的烧杯中,观察到铁钉表面有气泡产生,烧杯底部沉有固体物质。取出铁钉后用水清洗,铁钉恢复光亮。
Ⅰ.容器底部固体成分探究
(1)【实验探究1】取出容器底部剩余的固体物质,用水清洗后干燥,分成甲、乙两份。
| 实验操作 | 实验现象 | 解释与结论 |
| ①用磁铁靠近固体物质甲 | 固体物质________(选填“能”或“不能”)被吸引 | 固体物质中不含铁单质 |
| ②将固体物质甲放入20%的盐酸中 | 固体逐渐消失,溶液变成黄色 | 固体物质主要是氧化铁,反应的化学方程式为________ |
①固体物质
(选填“能”或“不能”)被吸引;
②固体物质主要是氧化铁,反应的化学方程式为
。
Ⅱ.溶液中逸出气体成分探究
【猜想假设】气体中除了可乐本身含有的CO
2外,可能还有H
2。
【查阅资料】
①H
2可以还原CuO,生成Cu和H
2O
②无水硫酸铜为白色固体,遇水变蓝。
③碱石灰做干燥剂,防止空气成分干扰。
【实验探究2】将逸出气体依次通过如图所示的组合装置。
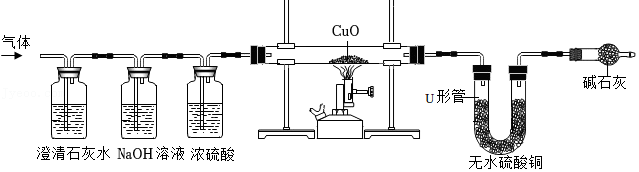
(2)NaOH溶液的作用是
。
(3)实验过程中观察到
现象,证明逸出气体中含有氢气。
Ⅲ.拓展延伸
铁钉表面已变光亮,而容器底部有大量铁锈剩余的原因是什么?可能是可乐酸性弱,与铁锈反应太慢。
【查阅资料】3%的稀盐酸pH约为1,该品牌可乐的pH为3.39。
【实验探究3】取另一份固体物质乙放入3%的稀盐酸中,振荡,观察到无明显现象。
(4)【实验结论】对比【实验探究1】和【实验探究3】的不同反应现象可得出化学反应速率与反应物的
有关。
(5)【合理推测】可乐能快速去除铁钉表面铁锈的真正原因是铁锈结构疏松多孔,
。