19.请根据如图a、b、c三种固体的溶解度曲线,回答下列问题:
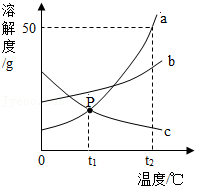
(1)a、b、c三种物质溶解度与温度的变化关系类似气体溶解度的是
。
(2)t
2℃时,配制60g的a物质的饱和溶液,需称量a的质量
g。
(3)若b物质中混有少量a物质,最好采用
的方法提纯b(填“降温结晶”或“蒸发结晶”)。
(4)下列说法正确的是
。
A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减少
B.t
2℃时,a、b、c三种物质的饱和溶液各100g,降温至t
1℃,所得溶剂的质量由大到小的顺序c>b>a
C.将t
1℃时c物质的饱和溶液升温到t
2℃,其溶液的质量一定减少
D.将t
1℃时a、b、c的饱和溶液升温至t
2℃,所得溶液溶质质量分数大小关系为b>a>c
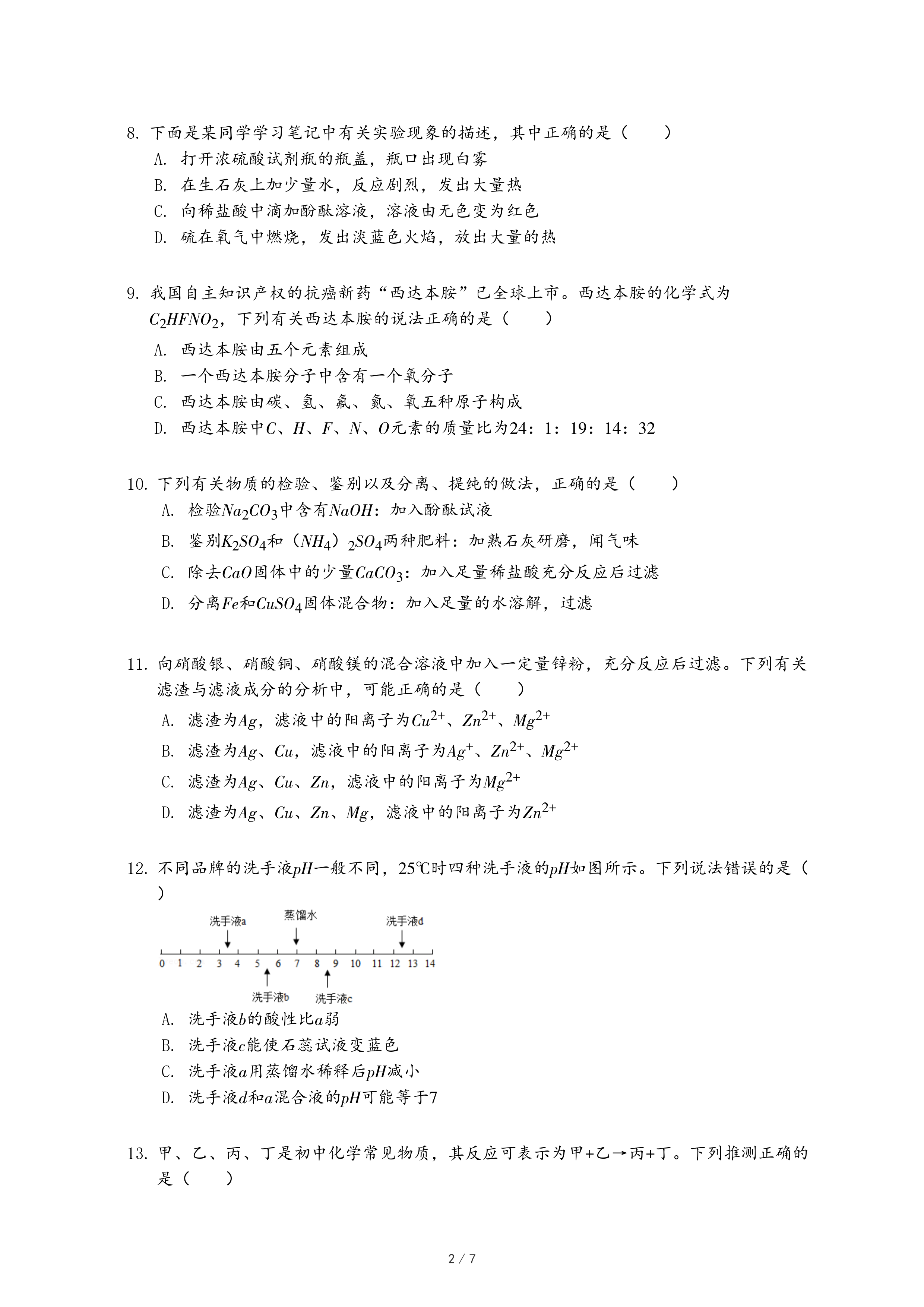



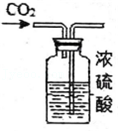 干燥CO2
干燥CO2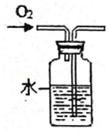 监控O2流速
监控O2流速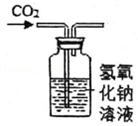 吸收CO2
吸收CO2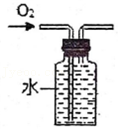 收集O2
收集O2