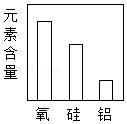
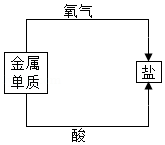
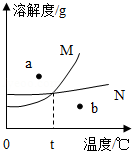
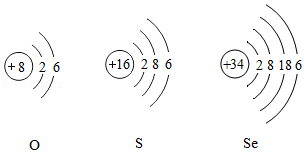
17.化学老师演示了一个"黑面包"实验:往烧杯中倒入蔗糖和少量水,再注入一定量的浓硫酸,用玻璃棒迅速搅拌,可观察到蔗糖迅速变黑,并逐渐膨胀成"面包"状,同时烧杯壁明显发烫并有大量水雾。同学们对这个实验进行了探究:
【査阅资料】SO
2有则激性气味,与CO
2一样能与NaOH溶液反应,也能让澄清石灰水变浑浊。此外,SO
2还易被酸性KMnO
4吸收,并能让品红(一种红色试剂)褪色。
探究一:黑色物质
(1)蔗糖(C
12H
22O
11)脱水的反应为C
12H
22O
11 12X+11H
2O,则黑色物质X为
。
探究二:面包的成因
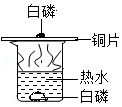
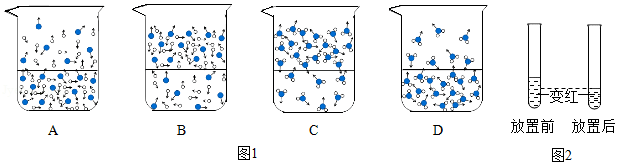
(2)如图1组装装置,滴入浓硫酸后气球膨胀,冷却至室温后,观察到气球
,甲同学据此认为膨胀不仅是由于放热造成的,还生成了气体。
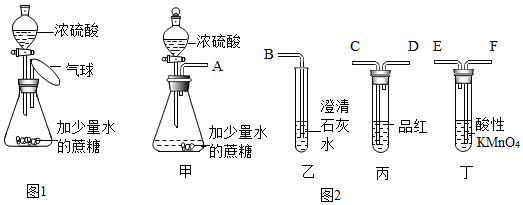
探究三:生成的气体
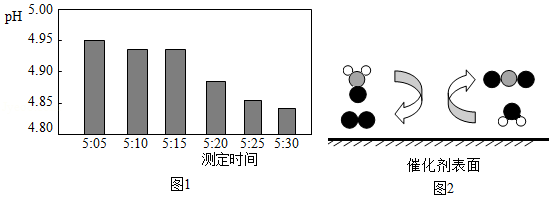
(3)乙同学将气求摘去并将图2甲、乙装置相连后,重新进行实验时发现石灰水变浑浊,并能闻到刺激性的气味,他判断生成了SO
2。
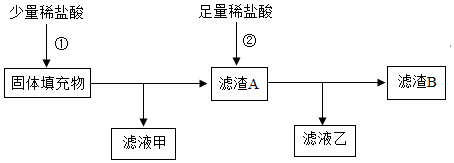
为了确认是否还生成CO
2,乙同学认为要避免干扰,先确保除尽SO
2,再检验CO
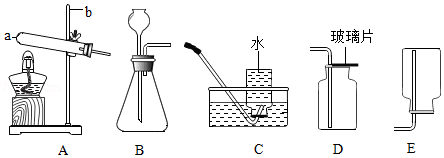
2,则需按气流由左向右流向:A﹣
、
、
、
﹣B连接好装置。能说明气体产物中有CO
2的实验现象是①品红溶液
②澄清石灰水浑浊。
由此说明面包膨胀的主要原因是黑色物质和浓硫酸反应产生了CO
2和SO
2,请将该反应的化学方程式补充完整:
+2H
2SO
4(浓)
。
(4)丙同学考虑到可能还会生成有毒气体CO,在参考乙同学的思路下设想用如图3所示的装置进行证明。则A、B中的试剂应分别为
(填标号)。
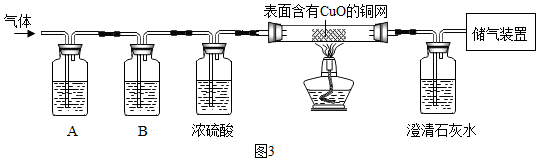
A.NaOH溶液、石灰水
B.石灰水、NaOH溶液
C.酸性KMnO
4溶液、石灰水