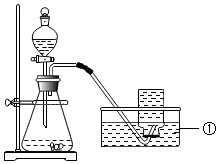
19.实验课上,同学们以“鉴别氢氧化钠、碳酸钠、稀硫酸、氯化钠”为题展开实验,并探究其反应后液的成分。
【讨论交流】同学们经过讨论,认为物质鉴别的原理是:依据物质的性质,选择合适试剂或药品,通过产生不同的现象来区分不同的物质,于是设计了如下步骤。
步骤1:利用pH试纸鉴别出稀硫酸和氯化钠。请写出测定溶液pH的操作
。
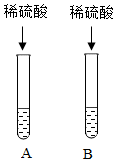
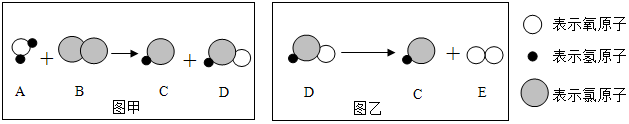
步骤2:利用稀硫酸鉴别碳酸钠和氢氧化钠(如图所示)。
【实验探究】(1)同学们在鉴别碳酸钠和氢氧化钠时,观察到试管B中有气泡产生,则试
管B中发生反应的化学方程式为
。
(2)实验中试管A未观察到明显现象,为证明试管A中已发生化学反应,同学们又设计了如下两种方案:
| | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量反应后的液体于试管中,加入适量BaCl2溶液 | 有白色沉淀产生 | 试管A中已发生化学反应 |
| 方案二 | 取少量反应后的液体于试管中,加入几滴酚酞溶液 | 溶液为无色 |
小云同学对方案一产生质疑,理由是
。
(3)实验后,同学们将A、B两支试管中的溶液倒入同一个大烧杯中,混合过程中观察到有气泡产生,同学们对烧杯中溶液的溶质成分产生了兴趣,作出了如下猜想并设计实验进行探究。
【作出猜想】猜想①:只含有Na
2SO
4猜想②:含有Na
2SO
4、Na
2CO
3猜想③:含有Na
2SO
4、NaOH、Na
2CO
3猜想④:含有Na
2SO
4、H
2SO
4请指出上述4种猜想中不合理的猜想并说明原因:
。
【进行实验】同学们设计了如下实验进行探究:
| | 实验步骤 | 实验现象 | 实验结论 |
| 活动一 | 取少量烧杯中的溶液于试管中,加入Ba(NO3)2再加入少量稀硝酸 | 有白色沉淀产生,加入稀硝酸后,沉淀部分溶解 | 溶液中含有Na2CO3,猜想②成立 |
| 活动二 | 取少量烧杯中的溶液于试管中加入稀盐酸 | | 溶液中含有Na2CO3,猜想②成立 |
| 活动三 | | 无明显现象 | 溶液中不含H2SO4猜想④不成立 |
【反思评价】
(1)小凌同学分析实验时,认为没有必要做活动三就能得到正确结论,其原因是
。
(2)实验结束后为防止实验产生的废液直接排放后污染环境你认为应该向废液中加入适量
处理达标后才能排放。



 侯德榜
侯德榜 道尔顿
道尔顿 门捷列夫
门捷列夫 拉瓦锡
拉瓦锡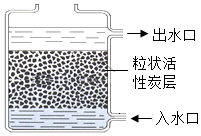 活性炭净水
活性炭净水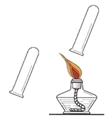 检验氢气的纯度
检验氢气的纯度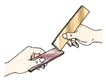 比较合金和纯金属的硬度
比较合金和纯金属的硬度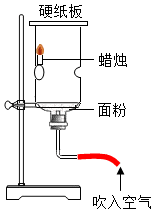 验证粉末爆炸
验证粉末爆炸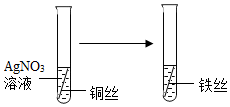



 。
。