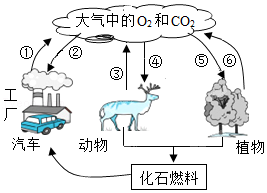
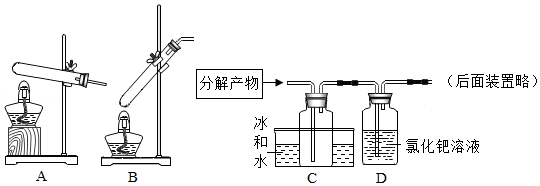
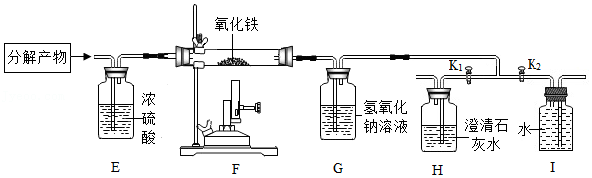
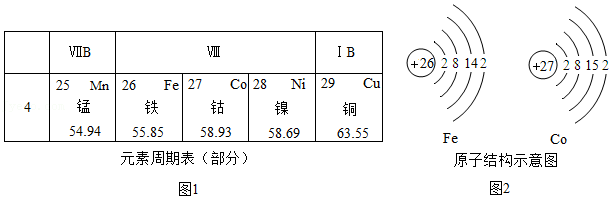
14.小倩同学了解到:外国人把中国称为China,在英文中与瓷器是同一个单词,“青花瓷”又是在中国瓷器中最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。她查阅元素周期表发现钴(读音:gǔ)元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
(提出问题)小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
(寻求帮助)
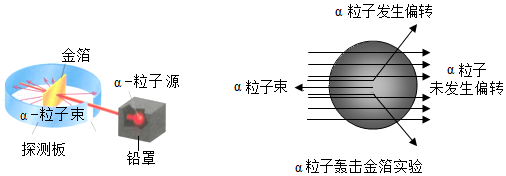
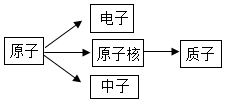
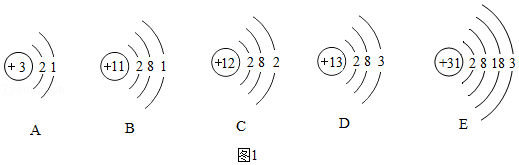
(1)(咨询老师)得知:因为铁与钴两种元素原子的结构具有相同点(见如图2),使得二者的化学性质相似。因此把这两种元素放在一起。请你帮助小倩完成下列问题:
①钴元素在元素周期表中的原子序数为
,一个钴原子比一个铁原子多一个
(填序号)。
a.中子
b.电子
c.质子
d.电子层
②铁原子与钴原子具有相同的
(填序号,下同)。元素的化学性质主要与原子的
有关,因此二者的化学性质相似。
a.核电荷数
b.核外电子数
c.电子层数
d.最外层电子数
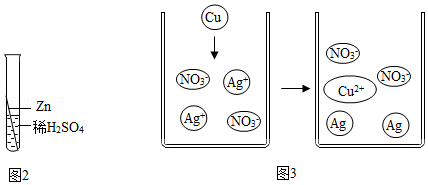
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为:
。钴在氧气中燃烧生成Co
3O
4,化学方程式为
。
(2)(查阅资料)钴元素有着广泛的用途:钴及其化合物在材料生产、化工生产、医疗中都有着广泛的应用。钴在电池制造中需求量增长很快,钴酸锂(已知:化学式为LiCoO
2,锂元素化合价为+1)常用作手机电池的正极材料,其中钴元素的化合价为
。
(深入探讨)(产生问题)既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
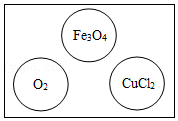
(设计并实验)(1)根据所学知识,同学们已知下列反应可以进行,并进行实验:
FeO
FeCl
2Fe(OH)
2观察记录实验现象:氧化亚铁为黑色固体:实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。
(查阅资料得知:原因是溶液中的Fe(OH)
2遇空气中的氧气生成Fe(OH)
3)
(2)同学们欲探究钴元素化合物的性质,设计并进行了如下实验:
CoO
CoCl
2Co(OH)
2请你依据实验现象,完成下列问题:
Ⅰ.实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式
。另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解溶液呈绿色。说明反应后钴离子在溶液中呈现的颜色与加入酸的
有关。
Ⅱ.实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的
有关。通过实验探究,同学们得出结论:铁和钴两种元素的化合物化学性质相似。



 闻气体气味
闻气体气味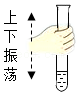 振荡试管
振荡试管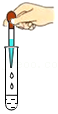 滴加液体药品
滴加液体药品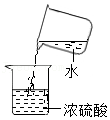 稀释浓硫酸
稀释浓硫酸