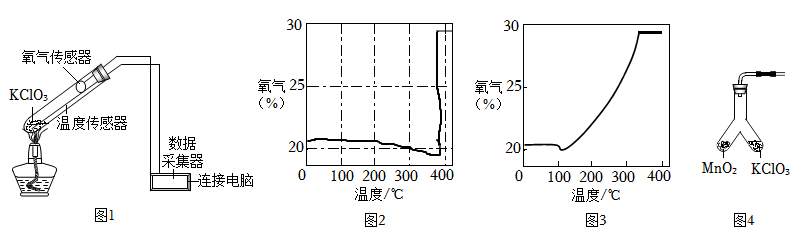
17.某兴趣小组对氯酸钾制取氧气中二氧化锰的催化作用进行探究。
(1)【查阅资料】
氯酸钾是
色固体,熔点约为356℃;二氧化锰的分解温度约为535℃;用酒精灯给物质加热,受热物质的温度约为400℃。
【实验1】
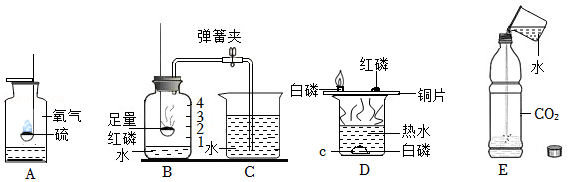
实验装置如图1所示(略去夹持装置)。氯酸钾分解时,传感器测得氧气浓度随温度的变化曲线如图2,加入二氧化锰作催化剂(氯酸钾与二氧化锰的质量比为4:1)后氧气浓度随温度的变化曲线如图3。
根据图回答问题:
(2)由图2可知,氯酸钾分解温度
(填“>”、“=”或“<”)其熔点;在氯酸钾分解前,传感器测得氧气浓度降低的原因可能是
;该反应的化学方程式为
。
(3)由图3可知,当氯酸钾与二氧化锰的质量比为4:1时,氯酸钾分解温度约为
℃。
【实验2】
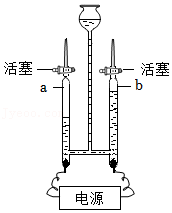
(4)为证实二氧化锰的催化作用,他们利用如图4装置进行实验,记录如表:
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 实验前,检查气密性,操作方法是________。 | ________ | ________ |
| Ⅱ | 分别在“Y”形管两侧支管中加入少量二氧化锰和氯酸钾,塞紧橡皮塞。 | / | ________ |
| Ⅲ | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星的木条放在导管口。 | 加热左侧(MnO2)支管,可观察到________,加热右侧(KClO3)支管,可观察到________。 |
| Ⅳ | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热,用带火星的木条放在导管口。 | 除了产生气体的时长不同外,其他现象同步骤Ⅲ的________。 |
(5)【评价与反思】
小组讨论后认为得出以上实验结论前,还需证明此反应中二氧化锰的
和
不变。



 量取液体
量取液体 滴加液体
滴加液体 闻气味
闻气味 熄灭酒精灯
熄灭酒精灯