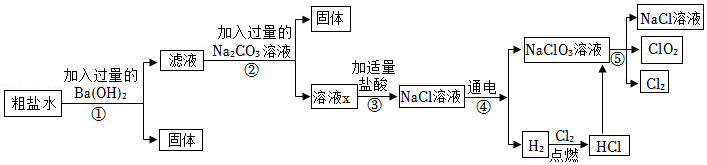
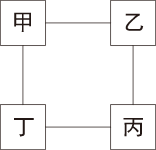
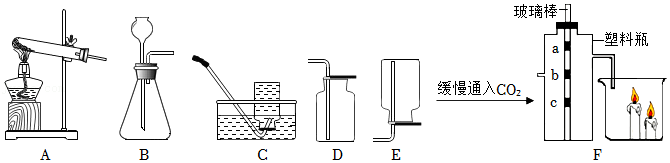
17.某同学春游时带了一包自加热食品,进餐时不用火,不用电,就能享用美味。同学们对该自加热食品产生了强烈兴趣,于是进行了如下实验探究。
【查阅资料】发热包中物质的主要成分是生石灰、活性炭、铝粉、铁粉、碳酸钠;铝粉能与氢氧化钠溶液反应,产生H
2。
探究一:发热包的发热原理。
(1)将发热包中固体倒入烧杯中,加入适量水,发生剧烈反应,水很快沸腾。写出该过程中生石灰与水反应的化学方程式:
,反应结束后,烧杯底部有大量固体,继续加水搅拌,过滤、洗涤、干燥,得到固体混合物。
探究二:固体混合物的成分。
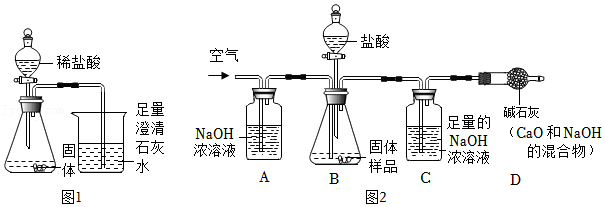
【设计实验】
(2)取少量固体混合物于试管中,加水振荡,静置,滴入几滴酚酞溶液,溶液变为红色,证明固体混合物中含有
。
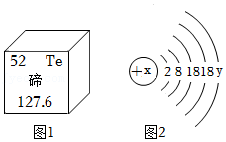
(3)另取少量固体混合物于锥形瓶中(如图1),加入过量稀盐酸充分反应。同学们观察到锥形瓶底部有剩余固体,溶液变浅绿色,烧杯中澄清石灰水变浑浊。证明固体混合物中含有
;若将分液漏斗中稀盐酸替换成氢氧化钠溶液,在滴加过程中无明显现象,证明固体混合物中
。
探究三:发热包中碳酸钠的质量分数。
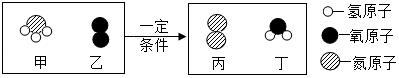
【设计实验】同学们设计并进行了如图2所示的实验。(装置气密性良好)
(4)【实验结论】实验前准确称取mg样品,实验完成后测得A装置增重ag,C装置增重bg,则样品中碳酸钠的质量分数为
(用含上述有关字母的代数式表示)。
【实验反思】
(5)实验过程中需持续缓缓通入空气,其作用有:搅拌B、C中的反应物,使其充分反应和
。
(6)若没有A装置,直接通入空气,则测得碳酸钠的质量分数
(填“偏大“、“偏小“或“不变“)。




 点燃酒精灯
点燃酒精灯 闻气体的气味
闻气体的气味 滴加液体
滴加液体 读取液体的体积
读取液体的体积