25.小峰同学在体育课上腿部擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
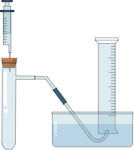
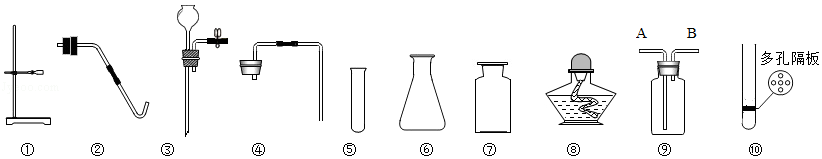
I.小峰准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
(1)请写出实验室中过氧化氢分解的化学方程式
。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到
,说明生成的气体是氧气。
II.小峰查阅了相关资料,并进行了探究实验。
【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 分两次进行实验,均注入5mL过氧化氢溶液,第一次在常温下进行,第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5mL | ________ |
| ② | 分两次进行实验,第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液,第二次________ | 第一次,量筒中2分钟收集到的气体体积为56mL;第二次,量筒中2分钟收集到的气体体积为__mL | 过氧化氢分解加快是因为过氧化氢酶的作用 |
(3)实验①得出的结论是
。
(4)实验②中“第二次”应进行的操作是
。
(5)实验②中第二次收集到的氧气体积为
mL。
【实验反思】
小峰反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
| | 加入过氧化氢酶 | 不加过氧化氢酶 |
| 反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
| 收集到气体体积/mL | 39 | 56 | 34 | 5 | 5 | 5 |
(6)通过这些数据,你能得出的新结论是
。