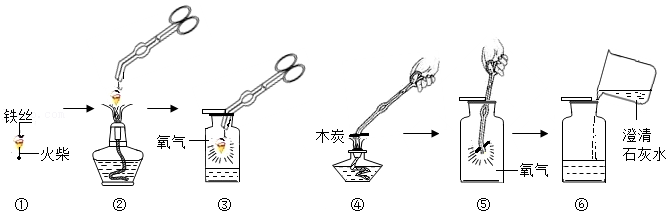
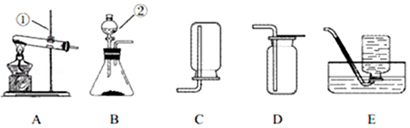
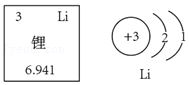
27.阅读下面短文。
| 乙醇(化学式:C2H5OH)俗称酒精,它是无色透明、具有特殊香味的液体,比水轻,沸点为78.5℃,易挥发;能与水任意比例互溶,能与乙醚、甲醇、丙酮等很多溶剂混溶,在空气中燃烧生成二氧化和水,同时放出大量的热。可用作酒精灯和内燃机中的燃料。乙醇是一种重要的化工原料,可用来制造醋酸、饮料、香精、染料等,医疗上也常用体积分数为70%~75%的酒精作消毒剂等。制备乙醇的方法很多,现在主要还是采用发酵法,把高粱,玉米等绿色植物的籽粒经过发酵,再进行蒸馏,就可以得到乙醇,在汽油中加入适量乙醇作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染,还可促进农业的生产。各种饮料酒里都含有酒精,如啤酒含酒精3%~5%,葡萄酒含酒精6%~20%,黄酒含酒精8%~15%,白酒含酒精50%~70%。酒精有加速人体的血液循环兴奋神经的作用,过量饮酒会造成酒精中毒,有害健康,因此要反对酗酒,未成年人不应饮酒,机动车驾驶员严禁酒后驾车。工业酒精约含乙醇96%,其中还常常有含有少量甲醇(化学式:CH3OH)。甲醇是无色易挥发有酒的气味的液体,易燃烧,燃烧产物也是二氧化碳和水,同时也放出大量的热。甲醇汽油是在甲醇中加变性醇添加,与现有国标汽油按照一定体积调配制成,它是一种低碳能源,可以替代普通汽油,是专门用于汽油内燃机机车使用的燃料。它具有替代性好、动力强,污染少等优点,具有良好发展前景。 |
依据短文内容,请回答下列问题。
(1)从组成元素上分析:乙醇是由
组成(填写元素种类)。从定量上分析:乙醇中碳元素的质量分数(C%)=
×100%=
×100%=26.9%。判断计算方法
(选“正确”或“错误”)。
(2)75%的医用酒精可以灭活新冠病毒,其溶质是
(填写化学式)。
(3)乙醇的物理性质①
②
(填写二条)。
(4)乙醇的用途①可用于医用消毒②
(不与①重复)。
(5)保存乙醇的要求:必须低温,避光,远离火源密封保存。简要解释必须“低温和避光、远离火源保存”的原因
。
(6)工业上采用发酵法制得乙醇,该过程通过发生
(选填“物理变化”或“化学变化”),实现对物质的改造。
(7)机动车驾驶员严禁酒后驾车,一种传统酒检测的原理是橙红色的重铬酸钾(K
2Cr
2O
7)的酸性水溶液遇到乙醇迅速生成绿色的硫酸铬Cr
2(SO
4)
3。根据是否变色及变色的变化程度,可以判断司机是否酒后驾车。该原理中,铬元素的化合价由+6变化为
。
(8)在汽油中加入适量乙醇作为汽车增料的社会意义是
(写一条即可)。
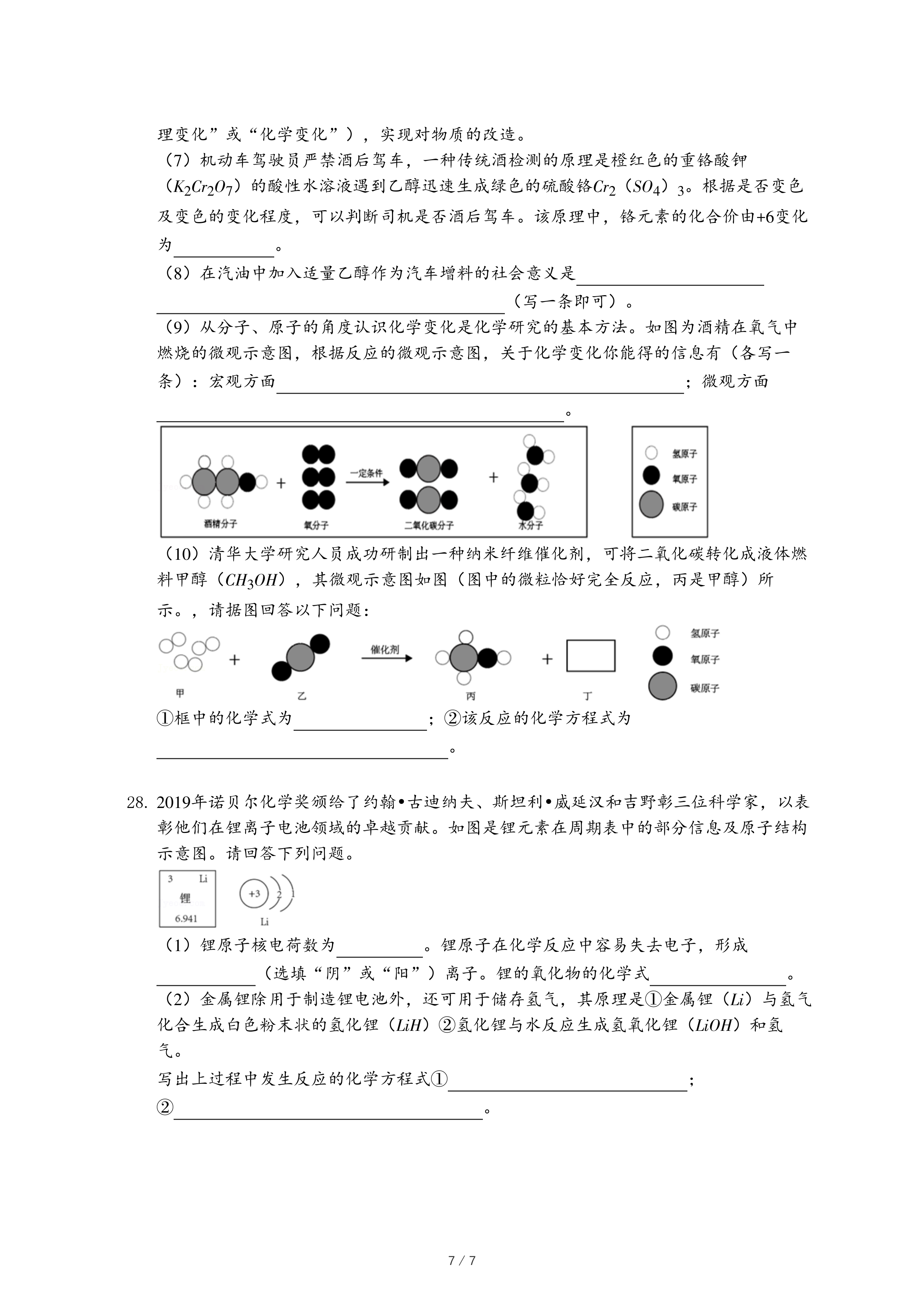
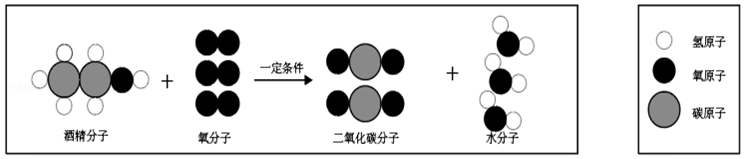
(9)从分子、原子的角度认识化学变化是化学研究的基本方法。如图为酒精在氧气中燃烧的微观示意图,根据反应的微观示意图,关于化学变化你能得的信息有(各写一条):宏观方面
;微观方面
。
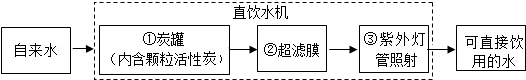
(10)清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇(CH
3OH),其微观示意图如图(图中的微粒恰好完全反应,丙是甲醇)所示。,请据图回答以下问题:
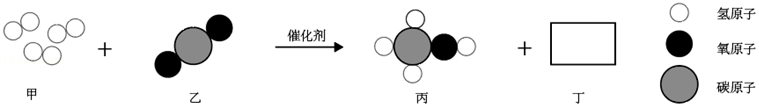
①框中的化学式为
;②该反应的化学方程式为
。