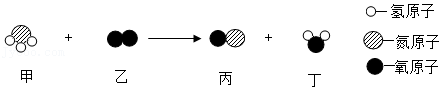
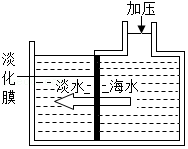
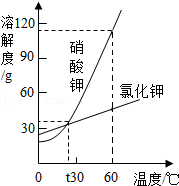
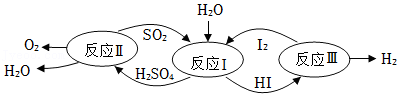
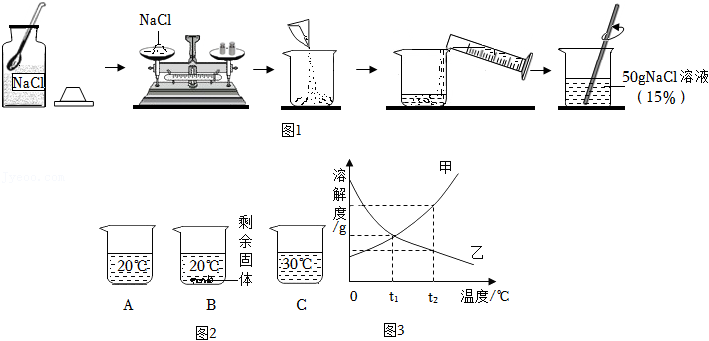
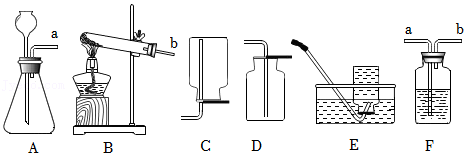
27.钢铁是日常生活中应用最为广泛的金属材料。
I、工业炼铁的原理是,高温下焦炭在高炉中生成的一氧化碳跟铁矿石反应生成铁。请回答下列问题:
(1)写出以赤铁矿为原料在高温下炼铁的化学方程式:
;
(2)加入焦炭,其作用除了可以生成一氧化碳外,还能
。
II、某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe
2O
3反应后的产物。所用装置如图所示。
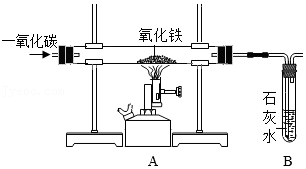
(3)如果实验成功,请回答下列问题:
①实验过程中产生的现象:
、
。
②B装置中发生反应的化学方程式
。
③该实验的操作步骤:
。
A点燃A处酒精喷灯
B.通入CO气体
C.停止通入CO气体
D.熄灭酒精喷灯
④该装置设计有一个明显缺陷,你认为是
。
实验时准确称取一定质量纯净的Fe
2O
3固体和相关装置的质量按上图进行实验,当固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。实验测得部分数据如下:
| | 玻璃管中固体的质量 | 装置B试管及其中物质的总质量 |
| 反应前 | 32g | 300g |
| 反应后 | 28.8g | 308g |
实验分析
查阅资料:
①Fe
2O
3与CO反应的固体生成物可能情况如下:
Fe
2O
3Fe
3O
4FeO(黑色)
Fe
②铁的氧化物在足量的稀盐酸中均能全部溶解;③石灰水只能吸收部分CO
2(4)实验结论:根据可靠实验数据计算得出反应后的黑色固体成分:
;此时玻璃管中发生的化学反应方程式:
。
(5)分析推断:①装置B试管中增加的质量一定会小于理论产生的CO
2质量,可能原因是
。
A.未参加反应的CO通过B时带走了水蒸气
B.石灰水浓度小没有将二氧化碳完全吸收
C.石灰水吸收了空气中的二氧化碳气体




 点燃酒精灯
点燃酒精灯 向试管中加入固体
向试管中加入固体 闻气体气味
闻气体气味 倾倒液体
倾倒液体