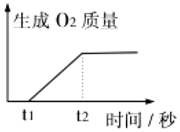
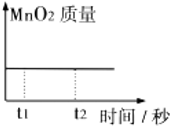
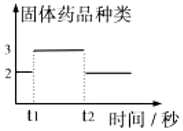
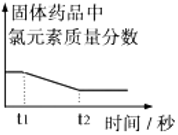
16.为定性、定量研究石灰石与稀盐酸反应,同学们仔细观察反应物质并查阅相关资料了解到,稀盐酸是氯化氢气体溶于水得到的无色溶液,石灰石主要成分是碳酸钙(白色),还含有一些不溶于水、不与稀盐酸反应的固体杂质,因杂质颜色不同导致石灰石的颜色也不尽相同,氯化钙易溶于水。
【实验前预测】同学们根据反应化学方程CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑推测反应现象主要有固体逐渐减小,但不会完全消失、
等现象。
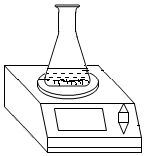
【定性研究】同学们检查完装置的气密性后,向大试管中加入3﹣4粒石灰石,倒约15mL稀盐酸,观察到了预测的现象,但也发现大试管内变浑浊这一异常现象,同时发现反应速率由快变慢直至反应停止。反应停止后,同学们又向上述试管中倒入相同浓度的稀盐酸约15mL,发现又开始反应,但第二次加同样的稀盐酸后反应速率明显比第一次要慢,把气体通入澄清的石灰水,石灰水变浑浊。
【深入研究】
(1)上述大试管内反应停止后,请设计一个实验证明稀盐酸是否反应完,实验方案
,可能的现象及结论
。
【定量研究】如图装置15.0克石灰石与120.0克稀盐酸混合,反应停止后,称得余下药品的质量为130.6克,老师说由此得出产生的二氧化碳的质量为15.0克+120.0克﹣130.6克=4.4克。
【反思交流】
(2)石灰水变浑浊反应的化学方程式为
。
(3)为什么第二次向大试管内加相同的稀盐酸时反应速率比第一次要慢,原因主要有两点:一是石灰石中的碳酸钙变少了,二是
。
(4)上述石灰石与稀盐酸反应的实验中,固体不会完全消失的原因是
,大试管内变浑浊的原因是
。
(5)有一同学对老师的说法提出了质疑,认为实际产生的二氧化碳的质量可能比4.4克大或小,也可能相等,理由是:
。





 表示氧原子,〇表示氢原子,↑表示运动方向),下列说法错误的是( )
表示氧原子,〇表示氢原子,↑表示运动方向),下列说法错误的是( )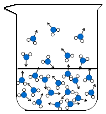
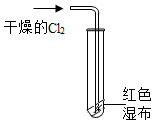
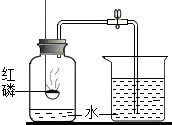 测定空气中氧气的含量
测定空气中氧气的含量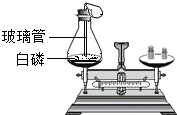 探究质量守恒定律
探究质量守恒定律 探究燃烧的条件
探究燃烧的条件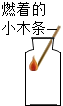 检验二氧化碳是否集满
检验二氧化碳是否集满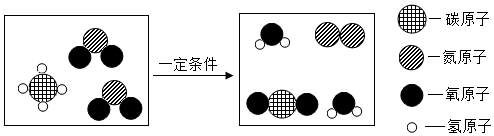

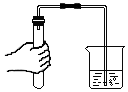 导气管放入水中,导管内液面低于烧杯内液面,或者手握试管,导管口有气泡
导气管放入水中,导管内液面低于烧杯内液面,或者手握试管,导管口有气泡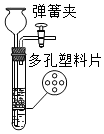 关闭弹簧夹,从长颈漏斗加水至浸没下端后再加适量水,长颈漏斗内液面与试管内液面相同
关闭弹簧夹,从长颈漏斗加水至浸没下端后再加适量水,长颈漏斗内液面与试管内液面相同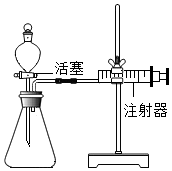 关闭分液漏斗活塞,向右拉动注射器活塞,松手后注射器活塞又弹回
关闭分液漏斗活塞,向右拉动注射器活塞,松手后注射器活塞又弹回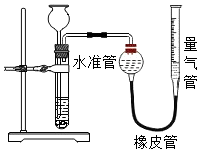 长颈漏斗加水至浸没下端,从量气管加水,水准管内液面低于量气管内液面
长颈漏斗加水至浸没下端,从量气管加水,水准管内液面低于量气管内液面