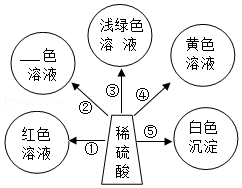
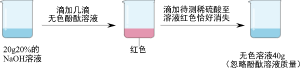
18.学习了常见的酸和碱后,同学们对碱的化学性质进行整理归纳并进行如下实验活动。
(1)【验证实验】
| 序号 | 实验一 | 实验二 | 实验三 | 实验四 |
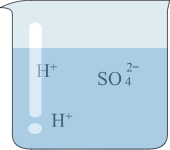
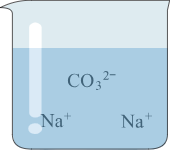
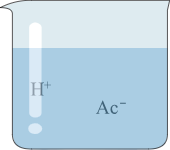
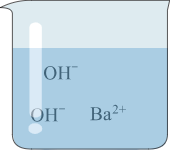
| 实验内容 | 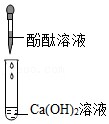 | 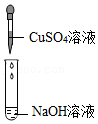 | 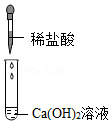 | 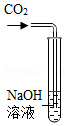 |
| 实验现象 | 溶液变 色 | 产生蓝色沉淀 | 无明显现象 | 无明显现象 |
| 分析与结论 | Ca(OH)2能与指示剂作用 | 反应的化学方程式为 | 无法确定是否发生反应 | 无法确定是否发生反应 |
请填写实验记录中空缺的内容。
【发现问题】
通过实验,同学们发现实验三、实验四无明显现象无法确定是否发生了化学反应。于是继续进行探究。
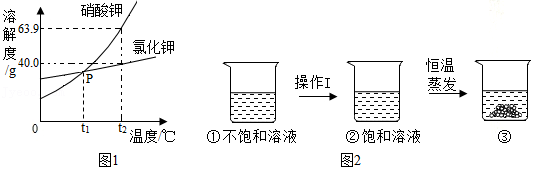
【探究实验】
(2)Ⅰ.取少量实验三中的剩余溶液,滴加
试液,溶液仍为无色,证明稀盐酸和Ca(OH)
2溶液发生了化学反应,判断依据是溶液中
完全反应了。
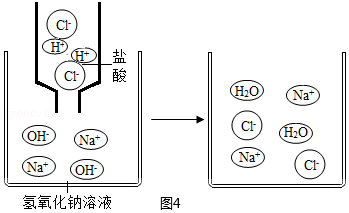
(3)Ⅱ.取少量实验四中的剩余溶液,滴加足量的
溶液,观察到产生气体,证明CO
2和NaOH溶液发生了化学反应。请写出产生气体的反应的化学方程式
。
【拓展延伸】
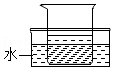
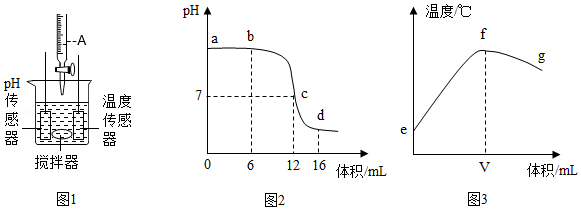
同学们针对实验四又进行了如图所示的对比实验:
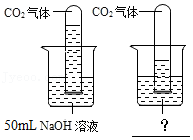
(4)Ⅲ.将充满CO
2的两支相同的试管分别倒扣入盛有不同液体(液体温度相同)的两个烧杯中,根据试管内液面上升的高度不同,确定CO
2和NaOH发生了化学反应。图中横线处对右侧烧杯中液体的说明应填写
;CO
2和NaOH发生反应的化学方程式为
。
【总结提升】
①通过上述实验验证了碱溶液的化学性质。
(5)②没有明显现象的化学反应,可以依据A检验反应物消失(或减少)或B。证明新物质生成这两种思路,利用间接观察法证明反应发生。上述三个实验分别是依据哪种思路设计实验方案的:Ⅰ
;Ⅱ
;Ⅲ
(填“A”或“B”)。



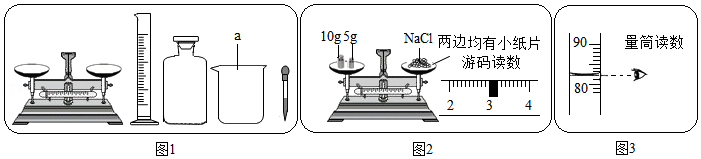
 测定溶液pH
测定溶液pH 配制溶液
配制溶液 称量固体
称量固体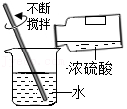 稀释浓硫酸
稀释浓硫酸