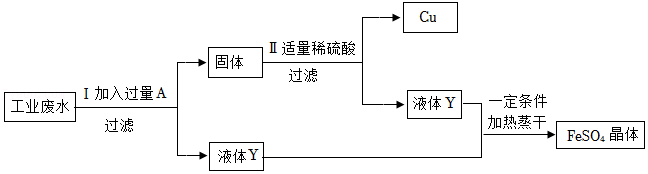
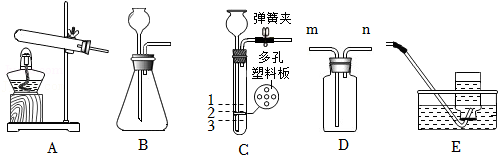
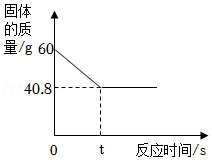
29.化学兴趣小组的同学用锌和稀硫酸进行实验制取氢气,发现不同组同学实验时反应速率有些差异。于是兴趣小组的同学们一起对“锌与硫酸反应速率的影响因素”进行探究,并利用下图装置收集产生的氢气。
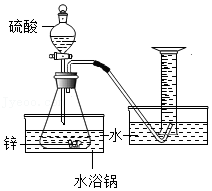
【查阅资料】圆粒状锌的直径通常为3﹣4毫米,粉末状锌的直径通常为0.3~0.5毫米。
(1)【作出猜想】同学们推测影响“锌与硫酸反应速率的影响因素”:
甲同学:温度;
乙同学:硫酸的溶质质量分数(即浓度);
丙同学:
。
【进行实验】同学们一起设计了如下实验方案进行实验。
| 编号 | 温度/℃ | 硫酸体积 | 硫酸溶质质量分数 | 锌的形状 | 锌的质量/g | 收集30mL氢气 |
| 1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
| 2 | 30 | 20 | 10% | 圆粒状 | 1 | 134 |
| 3 | 40 | 20 | 10% | 圆粒状 | 1 | 107 |
| 4 | 20 | 20 | 10% | 粉末状 | 1 | 47 |
| 5 | 20 | 20 | 20% | 圆粒状 | 1 | 88 |
| 6 | 20 | 20 | 20% | 粉末状 | 1 | 26 |
【解释与结论】
(2)锌与硫酸反应的化学方程式为
。
(3)能用排水法收集氢气的原因是氢气
(填“易”或“难”)溶于水。
(4)实验1、2、3的目的是探究
同学的猜想。
(5)欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比实验
(填编号)。
(6)通过对比实验5和实验6,得出的结论是
。
【反思与评价】
(7)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为
。
(8)将6.5g锌与100g19.6%的硫酸充分反应,可得到氢气
L(氢气密度为0.09g/L,精确到0.1L)




 倾倒液体
倾倒液体 放入锌粒
放入锌粒 检查气密性
检查气密性 铁丝在氧气中燃烧
铁丝在氧气中燃烧