






| 点燃 |
 仪器连接
仪器连接 滴加液体
滴加液体 振荡试管
振荡试管 倾倒液体
倾倒液体| 物质 | 液体肥皂 | 西瓜汁 | 胆汁 | 牛奶 |
| pH | 9.5~10.5 | 5.3~6.2 | 7.1~7.3 | 6.3~6.6 |

| 点燃 |
| 高温 |

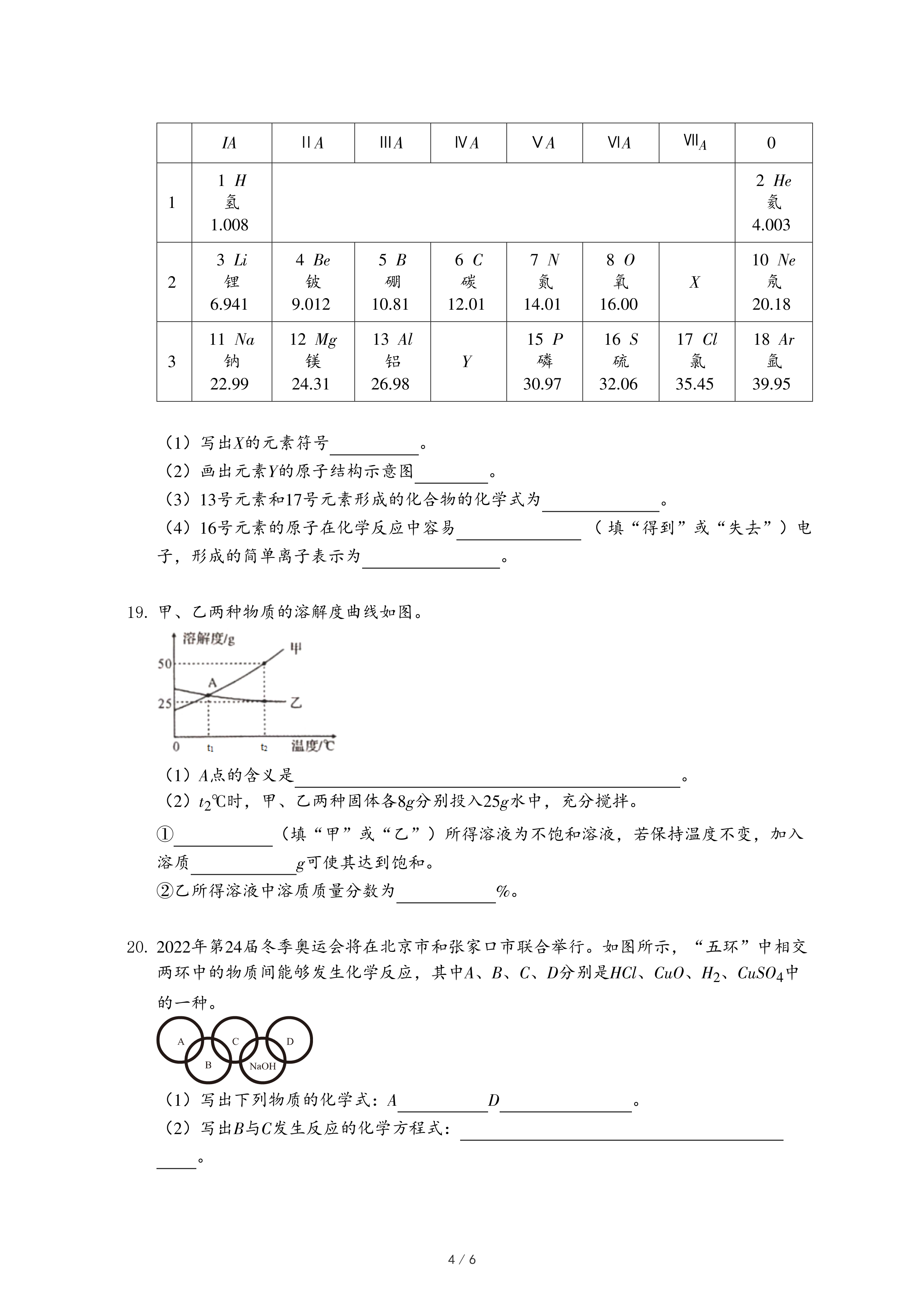
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | X | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | Y | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |




| 实验步骤 | 现象 | 结论 |
| 步骤Ⅰ:取少量滤液,向其中 加入足量盐酸溶液 | 猜想二不成立 | |
| 步骤Ⅱ:另取少量滤液,向其中 滴入适量Na2CO3溶液 | 产生白色沉淀 | 猜想 成立 |
