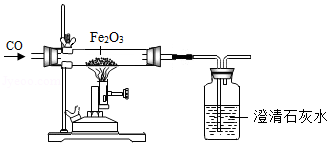
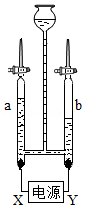
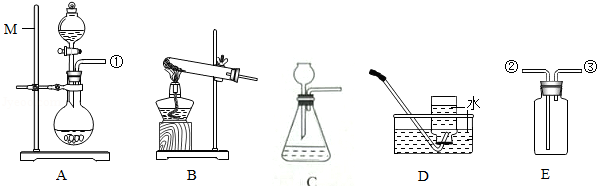
23.小李将实验剩余的FeCl
3溶液倒入含有H
2O
2的废液缸,立即产生大量的无色气泡。
(一)小李根据组成的元素猜测,无色气体可能是H
2、O
2、HCl、Cl
2中的一种或多种。
【查阅资料】1.Cl
2是黄绿色、有刺激性气味的气体
2.FeCl
3在水中解离出Fe
3+、Cl
﹣(1)根据资料,小李可排除的气体为
。
(2)【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察到木条燃得更旺,则该气体一定含
。
(二)小李认为上述过程中FeCl
3溶液作了H
2O
2分解的催化剂。
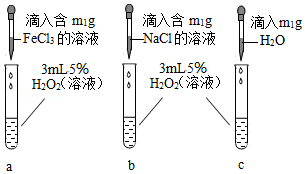
(3)【实验二】为进一步探究哪种离子起催化作用,他做了如图所示的对比实验。若要证明FeCl
3溶液中的Fe
3+对H
2O
2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为
。
(三)小王同学认为由此得出"FeCl
3溶液作H
2O
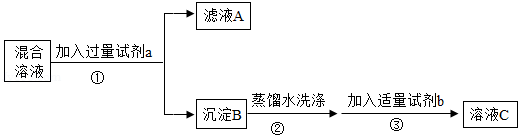
2分解的催化剂"的结论不严谨,还需要补充实验来进一步探究,他们又设计了如下实验:
【实验三】
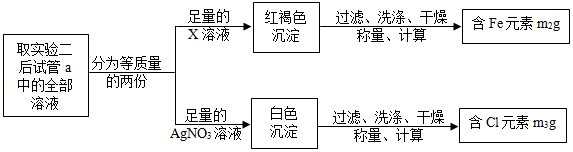
(4)X溶液中溶质的化学式为
。
【得出结论】要证明FeCl
3溶液作H
2O
2分解的催化剂,须满足以下两个方面的条件:
(5)从定性角度需观察到
(填序号)的现象。
A.实验一 B.实验二 C.实验三
(6)从定量角度需得到的关系式为m
1=
(用m
2和m
3表示)。



 取固体
取固体 称固体
称固体 量取水
量取水 溶解
溶解