



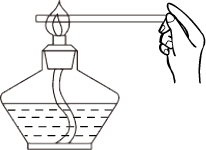
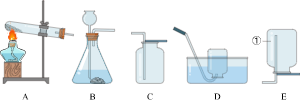
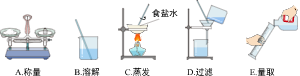
 引燃镁条
引燃镁条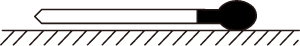 放置滴管
放置滴管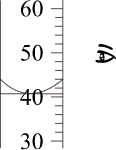 液体的量取
液体的量取 取用固体粉末
取用固体粉末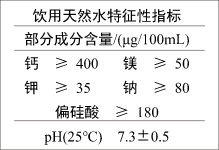

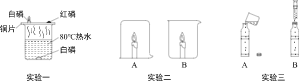
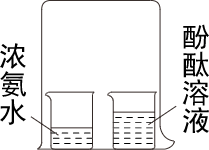 由酚酞溶液变红可知,分子是不断运动的
由酚酞溶液变红可知,分子是不断运动的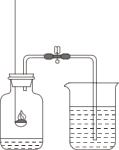 红磷量不足会使测量空气中氧气的体积分数偏大
红磷量不足会使测量空气中氧气的体积分数偏大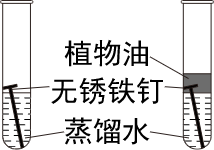 对照实验可得出铁生锈需要水和氧气
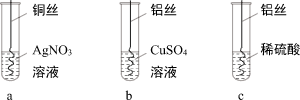
对照实验可得出铁生锈需要水和氧气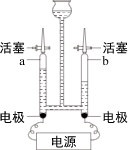 电解水实验在b管收集到的气体是氧气
电解水实验在b管收集到的气体是氧气| 高温 |
| 高温 |
| 选项 | 实验目的 | 所选药品或方法 |
| A | 提纯:氯化钠溶液中混有少量硝酸钾 | 降温结晶 |
| B | 除杂:铁钉表面的铁锈 | 长时间浸泡在过量的稀盐酸中 |
| C | 检验:肥皂水的酸碱性 | 用玻璃棒蘸取肥皂水滴到pH试纸上 |
| D | 鉴别:氯化铵、氯化铜、硫酸钾 | 氢氧化钠溶液 |
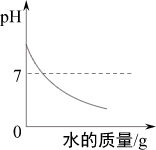 向氢氧化钠溶液中加水
向氢氧化钠溶液中加水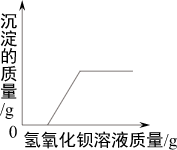 向一定量的HCl与Na2SO4混合溶液中不断加Ba(OH)2溶液
向一定量的HCl与Na2SO4混合溶液中不断加Ba(OH)2溶液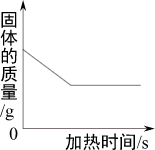 加热高锰酸钾
加热高锰酸钾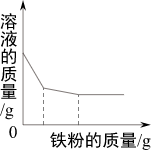 向一定质量的硝酸银和硝酸铜的混合液中加入铁粉
向一定质量的硝酸银和硝酸铜的混合液中加入铁粉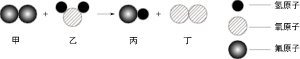
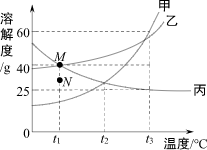
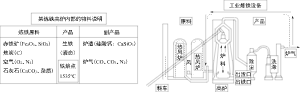
| 1 |
| 3 |

| 通电 |
| 实验操作 | 实验现象 | 实验结论 |
| 步骤a:取样溶于水,向溶液中滴加过量稀硝酸 | 杂质中含有碳酸钠 | |
| 步骤b:向a所得溶液中继续滴加硝酸银溶液 | 有白色沉淀产生 | 杂质中含有 |
