23.为认识酸和碱的性质,某化学学习小组进行了如下实验。
(1)20℃时,配制80g溶质质量分数为10%的NaOH溶液。
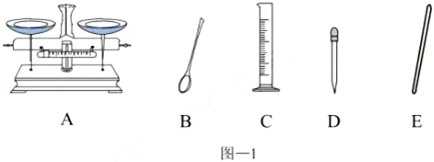
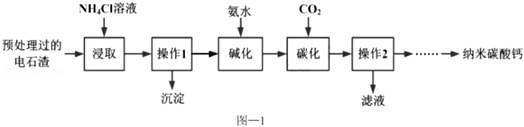
①用图﹣1中仪器完成实验,还缺少的玻璃仪器是
(填名称),玻璃棒在配制实验中的作用是
。
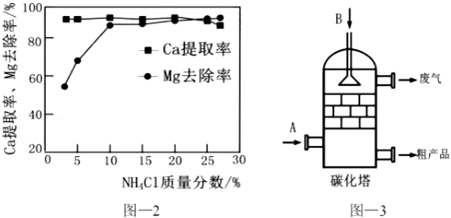
②配制该溶液需要
g水。用量筒量取水时,俯视读数会导致所配溶液的溶质质量分数
10%(填“大于”或“小于”)。
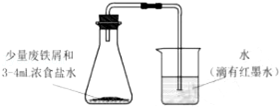
(2)向1~5 号小试管中分别滴加少量稀盐酸。
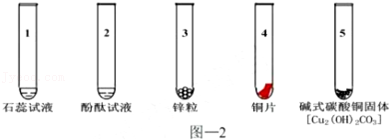
①
中溶液变为红色(填“试管1”或“试管2”)。
②试管3中产生气泡,试管4中无明显现象,由此推断金属活动性Cu比 Zn
(填“强”或“弱”)。
③试管5中生成一种盐和两种氧化物,该反应的化学方程式为
。
(3)借助传感器对稀NaOH溶液与稀盐酸的中和反应进行研究,实验装置如图﹣3,三颈烧瓶中盛放溶液X,用恒压漏斗匀速滴加另一种溶液。
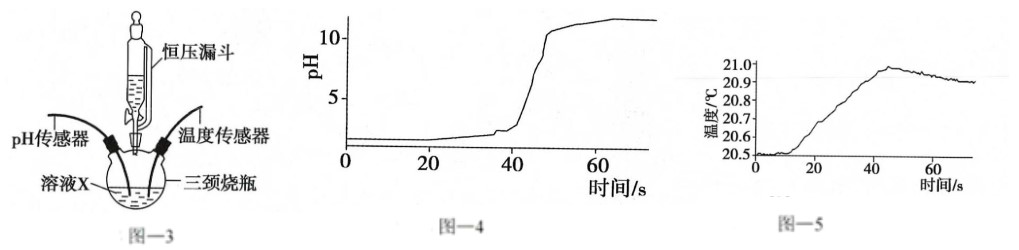
①甲同学用pH传感器测得三颈烧瓶内溶液pH的变化如图﹣4,判断溶液X是
,实验进行到60s时溶液中的溶质为
(填化学式)。
②乙同学用温度传感器测得三颈烧瓶内温度变化如图﹣5(实验过程中热量散失忽略不计),据此可得出反应过程中
能量的结论(填“吸收”或“释放”)。
③丙同学提出,通过监测三颈烧瓶内压强变化,也可以推导出乙同学的实验结论,其理由是
。
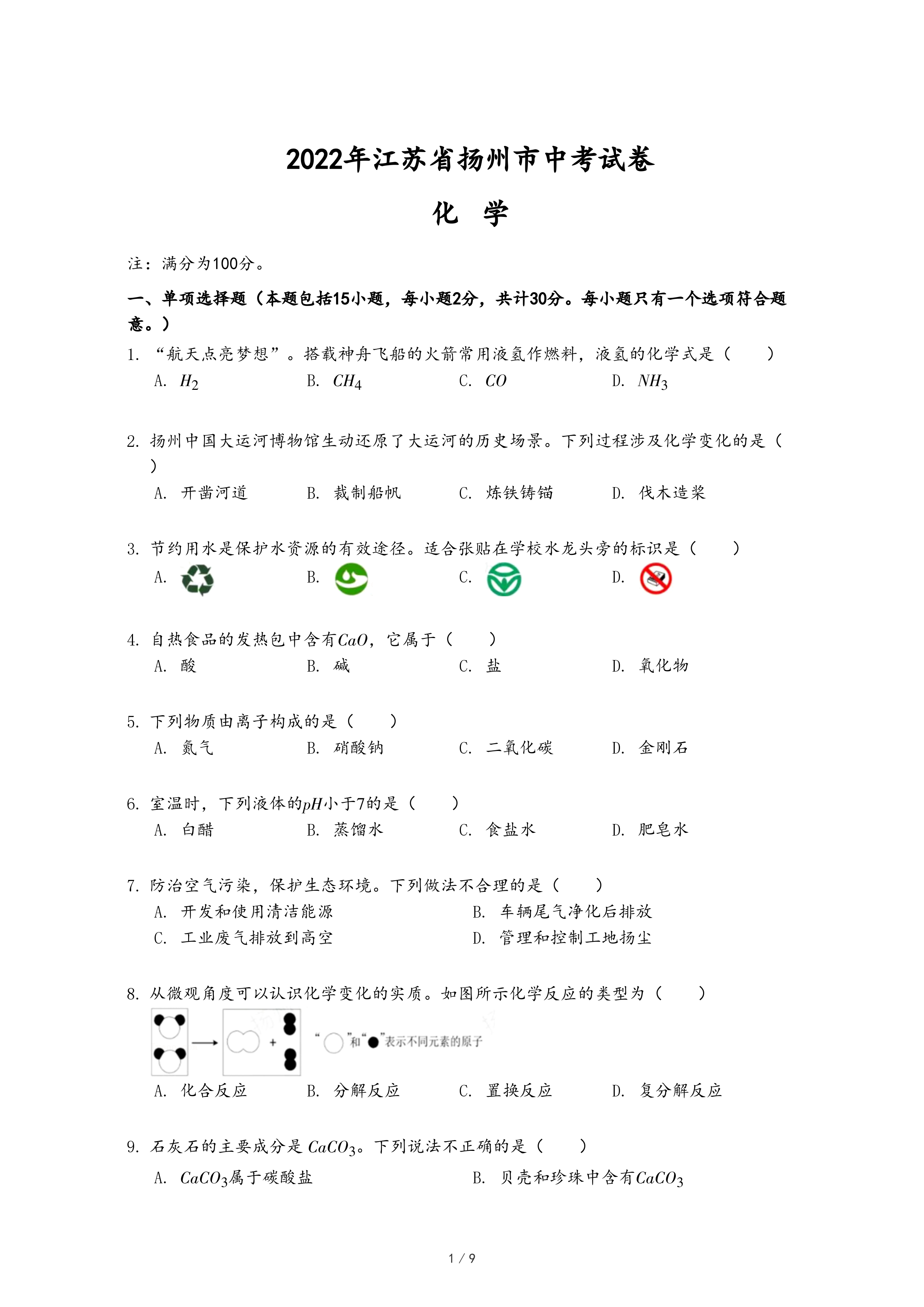







 检查装置气密性
检查装置气密性 加入石灰石
加入石灰石 收集CO2
收集CO2 验证CO2不支持燃烧
验证CO2不支持燃烧