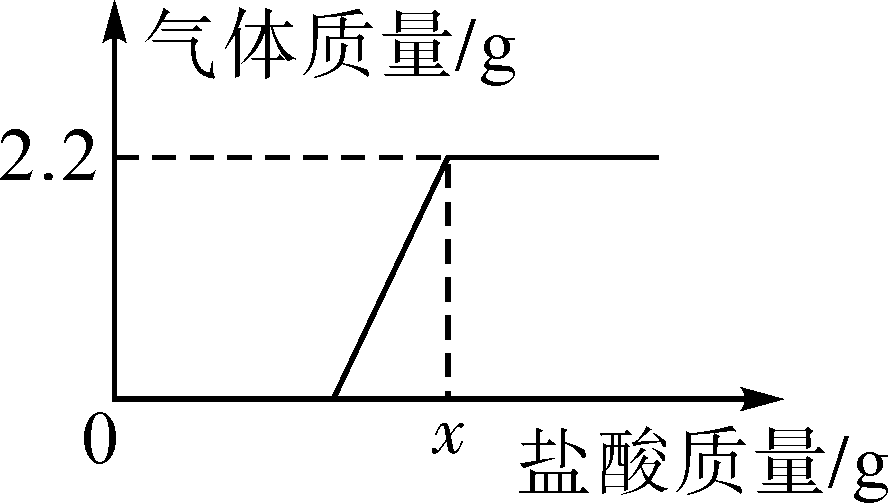
17.某化学兴趣小组在学习O
2制备时,对MnO
2做催化剂加快双氧水分解产生了兴趣,他们提出疑问:其他物质能否对双氧水分解速率产生影响?
【查阅资料】影响化学反应速率的因素有很多,如:使用催化剂、改变温度、改变反应物的浓度等。
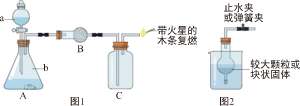
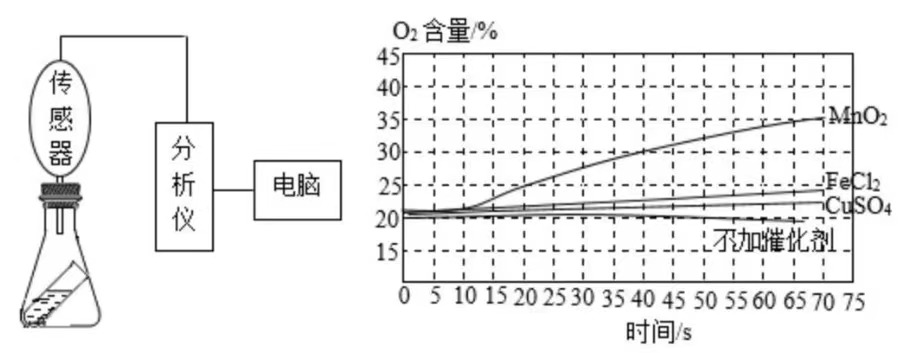
【实验探究】小组的同学们按图组装,在室温下分别进行了四组实验,并用O
2传感器测定实验过程中O
2含量的变化情况,得到如图所示曲线。
| 组别 | 试剂 |
| 第1组 | 2mL 5% H2O2 |
| 第2组 | 2mL 5% H2O2+3滴FeCl3溶液 |
| 第3组 | 2mL 5% H2O2+3滴CuSO4溶液 |
| 第4组 | 2mL 5% H2O2+少量MnO2粉末 |
【实验结论】对比四条曲线,进行分析:
(1)FeCl
3溶液、CuSO
4溶液对H
2O
2的分解
(填“有”或“无”)催化作用;
(2)几组实验中催化效果最优的H
2O
2分解的化学方程式
;
(3)第1组实验的目的是
;
(4)小组的同学们不加催化剂,在不同温度下,用不同浓度的H
2O
2进行实验,记录实验现象如表。据此可得出:升高温度或
(填“增大”或“减小”)反应物浓度可加快H
2O
2的分解。
| 温度H2O2% | 50℃ | 60℃ | 70℃ |
| 5% | 无明显气泡 | 无明显气泡 | 极少量气泡 |
| 10% | 无明显气泡 | 无明显气泡 | 少量气泡 |
| 15% | 无明显气泡 | 少量气泡 | 较多气泡 |
(5)实验需要30g10%的双氧水溶液,可用15%的双氧水溶液加
g蒸馏水配制。







 取用固体药品
取用固体药品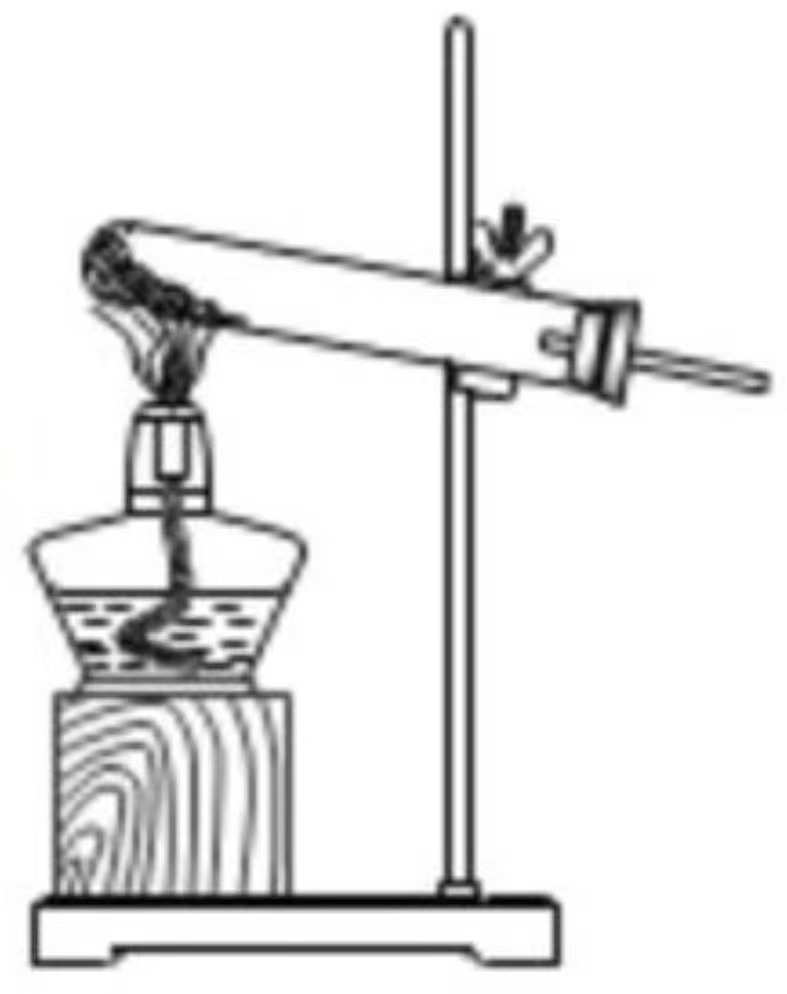 加热固体药品
加热固体药品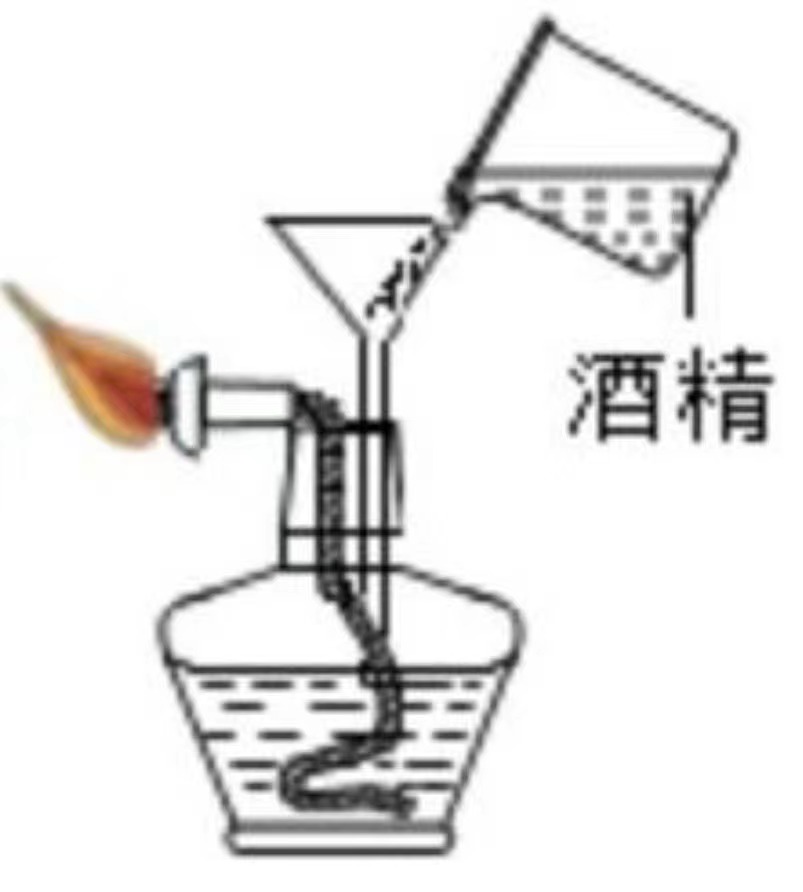 给酒精灯添加酒精
给酒精灯添加酒精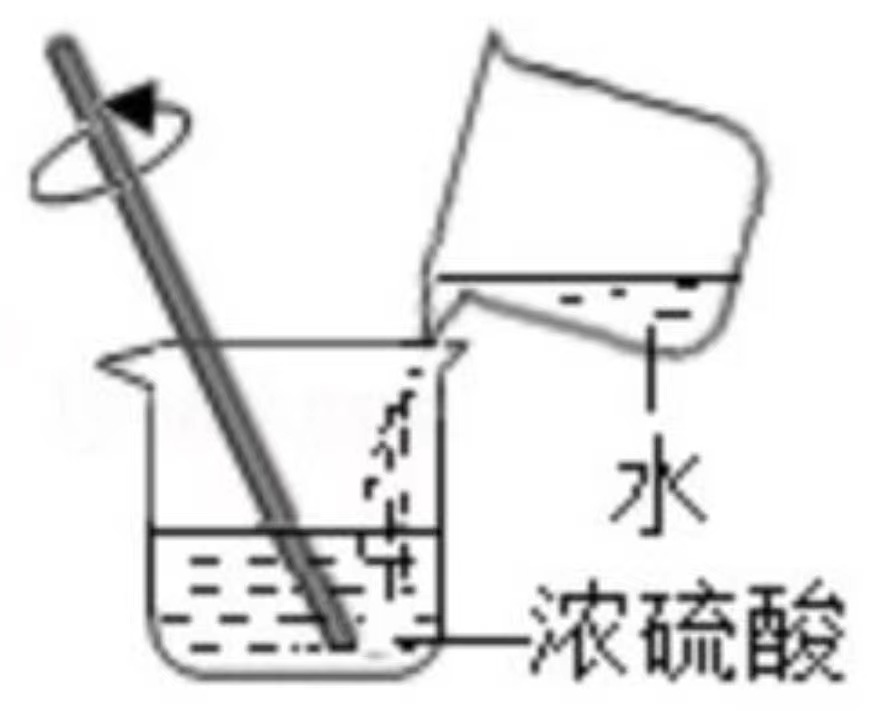 稀释浓硫酸
稀释浓硫酸