13.某兴趣小组同学在老师的指导下,进入实验室对碳酸钙进行了一系列探究。回答下列问题:
Ⅰ.碳酸钙与盐酸反应
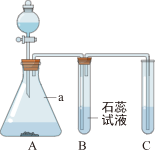
(1)装置A中仪器a的名称为
。
(2)装置B中的现象是
。
(3)装置C若用于检验生成的气体,其中试剂为
(写名称),发生反应的化学方程式为
。
Ⅱ.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
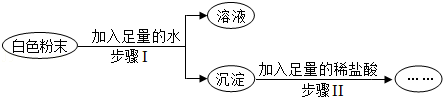
(4)【设计并完成实验】
| 实验操作 | 实验现象 | 解释与结论 |
| 步骤一:取剩余固体于试管中,加水振荡后静置 | 底部有白色不溶物 | \ |
| 步骤二:取上层清液于另一试管中,滴加氯化铜溶液 | 有 | 上层清液中一定含有氢氧化钙 |
| 步骤三:取部分底部白色不溶物于第三支试管中,滴加过量稀盐酸 | 有气泡产生 | 白色不溶物中一定含有 |
(5)【实验结论】正确的猜想是
。
(6)【交流与反思】小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是
(写一种即可);小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是
。
(7)【拓展与分析】查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物(CaO)的活性度,数据见如表。
| 煅烧温度活性度煅烧时间 | 1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ |
| 12 min | 790 | 836 | 868 | 808 | 454 | 412 |
| 16 min | 793 | 856 | 871 | 845 | 556 | 530 |
| 20 min | 795 | 863 | 873 | 864 | 617 | 623 |
石灰石煅烧的最佳温度范围一般为1100℃~1200℃的证据是
。



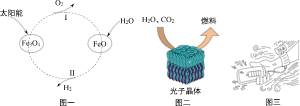
 “冰墩墩”——PET纤维
“冰墩墩”——PET纤维 场馆使用的太阳能电池——晶体硅
场馆使用的太阳能电池——晶体硅 速滑冰刀——钛合金
速滑冰刀——钛合金 冰壶——花岗岩
冰壶——花岗岩 取液
取液 加热
加热 稀释
稀释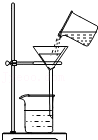 过滤
过滤